
分析 (1)根据含25%NaClO、密度1.19g•cm-3,及根据物质的量难度和溶质质量分数的换算公式c=$\frac{1000ρw}{M}$来计算;
(2)生产消毒液是将氯气通入NaOH溶液中生成氯化钠、次氯酸钠和水,据此书写离子方程式;
(3)①某同学欲用NaClO固体配制480mL含25%NaClO的消毒液,实验室中无480ml的容量瓶,需要在500ml的容量瓶中配制,固体配制溶液需要计算、称量、溶解、冷却转移、洗涤一并转移,加水定容,最后用胶头滴管定容到刻度,据此选择需要的仪器;
②依据配制过程分析,除上述仪器外,需要溶解和引流用到的玻璃棒;
③容量瓶带有磨口玻璃活塞,配制溶液过程中需要振荡摇匀,容量瓶需要倒立,玻璃活塞处需要防止漏液;
④根据C=$\frac{n}{V}$判断是否对配制溶液浓度有影响,如果n偏大或V偏小都导致C偏高.
解答 解:(1)某“84消毒液”的包装说明如下:含25%NaClO,密度1.192g•cm-3,该“84消毒液”的物质的量浓度c=$\frac{1000ρw}{M}$=$\frac{1000ml/L×1.192g/c{m}^{3}×25%}{74.5g/mol}$≈3.8mol/L,
故答案为:3.8;
(2)生产消毒液是将氯气通入NaOH溶液中反应生成氯化钠、次氯酸钠、水,发生的离子反应方程式为:Cl2+2OH-═ClO-+Cl-+H2O,
故答案为:Cl2+2OH-═ClO-+Cl-+H2O;
(3)①配制480mL含NaClO质量分数为25%的消毒液,应选取500 mL的容量瓶进行配制,所以需要NaClO的质量:0.5 L×4.0 mol•L-1×74.5 g•mol-1=149 g,固体配制溶液需要计算、称量、溶解、冷却转移、洗涤一并转移,加水定容,最后用胶头滴管定容到刻度,据此选择需要的仪器,称量固体需要用托盘天平、药匙,在烧杯中溶解,用玻璃棒搅拌加快溶解,冷却沿玻璃棒转移到500ml的容量瓶,洗涤一并转入,加水锂刻度线1-2cm处,改用胶头滴管滴加到刻度线,量筒可用可不用,•不需要的是100ml的容量瓶,
故答案为:B.
②上述分析可知除上述仪器外,还缺少的玻璃仪器是玻璃棒,
故答案为:玻璃棒;
③容量瓶带有磨口玻璃活塞,配制溶液过程中需要振荡摇匀,容量瓶需要倒立,玻璃活塞处需要防止漏液,所以容量瓶在使用前必须进行的一步操作是查漏,
故答案为:查漏;
④根据C=$\frac{n}{V}$判断是否对配制溶液浓度有影响
A.容量瓶是把溶质全部转移到容量瓶中,加水配制溶液到刻度线,所以配制前,容量瓶中有少量蒸馏水对配制溶液浓度无影响,故A不符合;
B.定容时俯视容量瓶刻度线,会导致加入水后未达到刻度线,使溶液浓度偏高,故B符合;
C.将溶解冷却后的溶液转入容量瓶后未洗涤烧杯和玻璃棒就进行定容操作,导致溶质损失,溶液浓度减小,故C不符合;
D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处,静置后得到溶液液面超出刻度线,浓度会偏低,故D不符合;
故答案为:B.
点评 本题考查物质的量浓度的计算以及溶液的配制,明确配制过程是解题关键,注意溶液稀释规律,侧重考查学生的分析能力、实验能力和计算能力的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 铜片插A硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| B. | 盐酸滴入澄清石灰水:Ca(OH)2+2H+═Ca2++2H2O | |
| C. | 将金属Na加入冷水中:2Na+2H2O═2Na+++2OH-+H2↑ | |
| D. | 向含0.5molFeBr2的溶液中通入0.5molC12:2Fe2++C12═2Fe3++2C1- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 物质 | 杂质 | 除杂质应选用的试剂和操作方法 | |
| A | CO2 | CO | 通入O2,点燃 |
| B | 乙醇 | 汽油 | 加入CCl4萃取、分液 |
| C | Cu(NO3)2溶液 | AgNO3溶液 | 加入过量的铜粉,过滤 |
| D | KNO3溶液 | KOH溶液 | 加入适量的CuSO4溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 150mL 2mol•L-1的KCl溶液 | B. | 75mL 4 mol•L-1的NH4Cl溶液 | ||
| C. | 75mL 1.5mol•L-1的MgCl2溶液 | D. | 150mL 1 mol•L-1的NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在海轮外壳上镶入锌块,可减缓船体的腐蚀速率 | |
| B. | 铁在潮湿的空气中容易腐蚀 | |
| C. | 镀锌的铁制品比镀锡的铁制品耐用 | |
| D. | 常温下铝跟稀硫酸快速反应,跟浓硫酸不反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通入CH4的电极为正极 | |
| B. | 放电时溶液中的阳离子向负极移动 | |
| C. | 负极的电极反应式为:CH4+10OH--8e-═CO32-+7H2O | |
| D. | 通入CH4的电极反应式为:CH4+2O2+4e-═CO2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
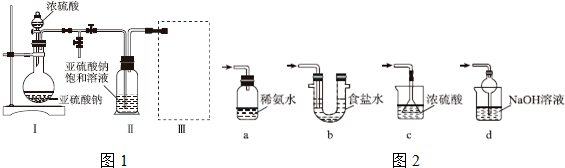

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用饱和NaHCO3溶液除CO2中的氯化氢气体 | |
| B. | SO2与乙烯的混合气体依次通入酸性高锰酸钾溶液、浓硫酸洗气后可得到纯净的SO2 | |
| C. | 用酒精萃取碘水中的碘单质 | |
| D. | 用CaO干燥Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com