
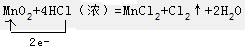
分析 (1)Mn元素的化合价由+4价降低为+2价,该反应中转移2e-,转移电子为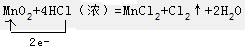 ;
;
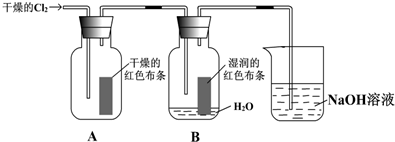
(2)Cl2与H2O反应生成HClO,反应的化学方程式为Cl2+H2O=HCl+HClO,具有漂白性的物质为HClO,则集气瓶B中湿润的红色布条褪色;
(3)氯气有毒,与氢氧化钠溶液反应,从而达到吸收尾气的作用;
(4)铁离子与铜单质发生氧化还原反应,离子反应方程式为:2Fe3++Cu=2Fe2++Cu2+;亚铁离子被氧化成铁离子,离子反应方程式为:2Fe2++Cl2=3Fe2++2Cl-.
解答 解:(1)Mn元素的化合价由+4价降低为+2价,该反应中转移2e-,转移电子为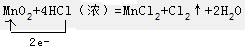 ;
;
故答案为:4H++2Cl-+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$Cl2↑+Mn2++2H2O;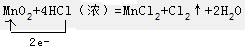 ;
;
(2)Cl2与H2O反应生成HClO,反应的化学方程式为Cl2+H2O=HCl+HClO,具有漂白性的物质为HClO,则集气瓶B中湿润的红色布条褪色,故答案为:褪色;干燥Cl2没有漂白性,Cl2与水反应生成 HClO有漂白性,Cl2+H2O?HCl+HClO;
(3)氯气有毒,与氢氧化钠溶液反应,从而达到吸收尾气的作用,故答案为:吸收尾气,防止污染空气;
(4)铁离子与铜单质发生氧化还原反应,离子反应方程式为:2Fe3++Cu=2Fe2++Cu2+;亚铁离子被氧化成铁离子,离子反应方程式为:2Fe2++Cl2=3Fe2++2Cl-,故答案为:2Fe3++Cu=2Fe2++Cu2+; 2Fe2++Cl2=3Fe2++2Cl-.
点评 本题考查HClO的漂白性的探究,题目难度不大,本题注意氯气与次氯酸性质的差异性,注意有关反应化学方程式或者离子方程式的书写,把握反应的原理.


 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:选择题

| A. | 维生素A属于烃 | |
| B. | 维生素A能发生取代、加成、酯化反应 | |
| C. | 维生素A不能使酸性KMnO4溶液褪色 | |
| D. | 维生素A不能与金属钠反应产生氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KSCN | B. | BaCl2 | C. | NaOH | D. | HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{4x-2y}{a}$ | B. | $\frac{2x-y}{a}$ | C. | $\frac{8x-3y}{2a}$ | D. | $\frac{8x-3y}{a}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②⑤ | B. | ②④ | C. | ①②⑤ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
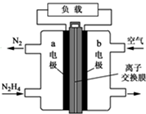 肼一空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景.其工作原理如上图所示,回答下列问题:
肼一空气燃料电池是一种碱性电池,无污染,能量高,有广泛的应用前景.其工作原理如上图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4 C2H4 | B. | CH4 C3H4 | C. | C2H4 C3H4 | D. | C2H2 C3H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
| Al2O3 | Si | Na2O2 | 水泥、玻璃、陶瓷 |
| 两性氧化物 | 单质 | 碱性氧化物 | 无机非金属材料 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com