
| A | ①能使溴的四氯化碳溶液褪色,常作植物生长调节剂; ②比例模型如图所示:  ③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成; ②球棍模型如图所示: 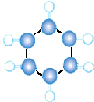 |
| C | ①C、H、O三种元素组成; ②与Na反应产生H2; ③与D反应可生成酯. |
| D | ①C、H、O三种元素组成,是厨房中的常见调味剂; ②水溶液能使紫色石蕊试液变红. |
分析 由表格中的信息可知,A为CH2=CH2,A与水加成生成C,C为CH3CH2OH,由B的球棍模型可知,B为苯,D的C、H、O三种元素组成,是厨房中的常见调味剂,水溶液能使紫色石蕊试液变红,可知D为CH3CHCOOH,C与D酯化反应生成CH3CHCOOCH2CH3,然后结合有机物的性质来解答.
解答 解:由表格中的信息可知,A为CH2=CH2,A与水加成生成C,C为CH3CH2OH,由B的球棍模型可知,B为苯,D的C、H、O三种元素组成,是厨房中的常见调味剂,水溶液能使紫色石蕊试液变红,可知D为CH3CHCOOH,C与D酯化反应生成CH3CHCOOCH2CH3,
(1)由以上分析可知A为CH2=CH2,C为C2H5OH或者CH3CH2OH,B为苯,分子式为C6H6,故答案为:CH2=CH2;C2H5OH或者CH3CH2OH;C6H6;
(2)D为乙酸,含有的官能团为羧基,故答案为:羧基;
(3))乙烯与溴反应生成1,2-二溴乙烷,方程式为CH2=CH2+Br2→CH2BrCH2Br,故答案为:CH2=CH2+Br2→CH2BrCH2Br;
(4)乙醇催化氧化反应生成乙醛,方程式为2CH3CH2OH+O2$→_{△}^{Cu/Ag}$ 2 CH3CHO+2H2O,故答案为:2CH3CH2OH+O2$→_{△}^{Cu/Ag}$ 2 CH3CHO+2H2O.
点评 本题考查有机物的推断、有机物结构与性质等,注意根据结构模型推断有机物,注意掌握官能团的性质与转化是关键,旨在考查学生对基础知识的掌握.


科目:高中化学 来源: 题型:实验题
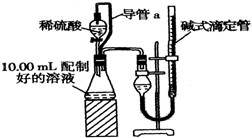
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 随着温度的升高,碳酸溶液的pH减小 | |
| B. | 随着温度的升高,纯水的pH减小 | |
| C. | 新氯水制经光照一段时间后,pH减小 | |
| D. | 氢氧化钠溶液久置于空气中,pH增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷、CO合成乙酸乙酯:2CH4+2CO$\stackrel{催化剂}{→}$CH3COOCH2CH3 | |
| B. | 烯烃与水煤气发生的羰基合成反应:RCH═CH2+CO+H2$\stackrel{催化剂}{→}$RCH2CH2CHO | |
| C. | 葡萄糖在酒化酶作用下转化为酒精 | |
| D. | 氯乙烯合成聚氯乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
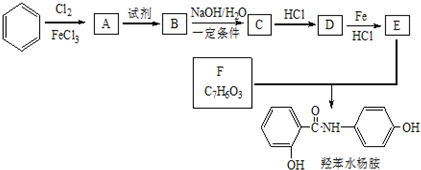
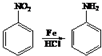
 +2NaOH$→_{一定条件}^{水}$
+2NaOH$→_{一定条件}^{水}$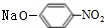 +NaCl+H2O.
+NaCl+H2O.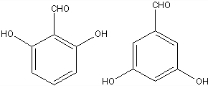 、
、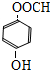 (任意一种).
(任意一种).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁和锌分别与相同浓度的盐酸反应,镁产生H2的速率快 | |
| B. | 铜与浓硝酸反应生成NO2,与稀硝酸反应生成NO | |
| C. | 用加热的方法可以将水中溶解的O-和N2赶出 | |
| D. | 面粉加工厂内充满粉尘,遇火易发生爆炸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌粒与稀硫酸的反应 | |
| B. | 甲烷在空气中燃烧的反应 | |
| C. | 灼热的木炭与CO2的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该原子中子数与质子数之差为 19 | |
| B. | 他们获得了一种新元素 | |
| C. | ${\;}_{26}^{45}$Fe与${\;}_{26}^{56}$Fe的化学性质几乎完全相同 | |
| D. | 这种铁原子衰变出 2 个质子后变成${\;}_{26}^{43}$Fe |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com