
【题目】下列是几种原子的基态电子排布,电负性最大的原子是
A. 1s22s22p4 B. 1s22s22p63s23p3 C. 1s22s22p63s23p2 D. 1s22s22p63s23p64s2
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】在两个容积相同的容器中,一个盛有HCl气体,另—个盛有H2和Cl2的混合气体。在同温同压下, 两容器内的气体一定具有相同的( )
A. 原子数 B. 密度 C. 质量 D. 质子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,装置Ⅰ为新型电池,放电时B电极的反应式为NaBr3+2Na++2e-===3NaBr,装置Ⅱ为铅蓄电池。首先闭合K1和K2,当铅蓄电池充电结束后,断开K1,闭合K2。下列说法正确的是( )
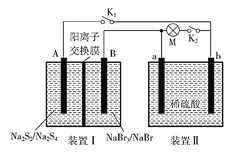
A. 闭合K1、K2时,每有0.1 mol Na+通过离子交换膜,装置II溶液中有0.1mol电子转移
B. 装置Ⅰ放电时的A电极反应式为2Na2S2-2e-===Na2S4+2Na+
C. 断开K1、闭合K2时,b电极的电极反应式为PbO2+2e-+SO42-+4H+===PbSO4+2H2O
D. 断开K1、闭合K2时,装置Ⅱ中SO42-向a电极迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】捕集、利用CO2是人类可持续发展的重要战略之一。
(1)用太阳能工艺捕获CO2可得炭黑,其流程如图所示:

①捕获1mo1CO2转移电子的物质的量是_________。
②过程2反应的化学方程式是________。
(2)将CO2催化加氢可合成低碳烯烃:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g),按投料比n(CO2):n(H2)=1:3将CO2与H2充入密闭容器,在0.1MPa时,测得平衡时四种气态物质,其温度(T)与物质的量(n)的关系如图所示。
C2H4(g)+4H2O(g),按投料比n(CO2):n(H2)=1:3将CO2与H2充入密闭容器,在0.1MPa时,测得平衡时四种气态物质,其温度(T)与物质的量(n)的关系如图所示。

①正反应的焓变△H_________0。
②提高CO2的转化率,可采用的方法是______。
a.增大n(CO2)与n(H2)的投料比
b.改变催化剂
c.缩小容器体积
③图中表示水的曲线是_____。
(3)电解CO2可制得多种燃料:下图是在酸性电解质溶液中,以惰性材料做电极将CO2转化为丙烯的原理模型。

①太阳能电池的正极是________。
②生成丙烯的电极反应式是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氦原子电子云图的说法正确的是( )
A. 通常用小黑点来表示电子的多少,黑点密度大,电子数目大
B. 黑点密度大小,表示单位体积内电子出现的机会多少
C. 通常用小黑点来表示电子绕核作高速圆周运动
D. 电子云图是对运动无规律性的描述
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求完成下列填空:
(1)质量之比为16∶7∶6的SO2、CO、NO分子个数之比为______。
(2)1.204×1024个D2O的质量为______。
(3)9.2g NOx中含有N原子数为0.2mol,则x数值为______。
(4) 1L1mol/L的AlCl3溶液中和1.5L______mol/L的MgCl2溶液中的氯离子浓度相等。
(5)在标准状况下,CO和CO2的混合气体共39.2 L,质量为61 g,则两种气体的物质的量之和为_______mol,其中CO2为__________mol。
(6)现有100mL 2mol/L的稀HCl溶液与足量的铁屑反应,将生成的FeCl2配成400mL溶液,此溶液中FeCl2的物质的量浓度是______________。
(7)在标准状况下,将224L氯化氢气体溶于635mL的水(密度为1g/cm3)中,所得盐酸的密度为1.18g/cm3,该盐酸中溶质的质量分数____________,该盐酸的物质的量浓度_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中属于氧化还原反应,但不属于四种基本反应类型的是 ( )
A. CuO + H2 ![]() Cu + H2O B. Fe2O3 + 3CO
Cu + H2O B. Fe2O3 + 3CO ![]() 2Fe + 2CO2
2Fe + 2CO2
C. 2KMnO4 ![]() K2MnO4 + MnO2 + O2↑ D. NaOH + HCl = NaCl + H2O
K2MnO4 + MnO2 + O2↑ D. NaOH + HCl = NaCl + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组微粒按半径逐渐增大,还原性逐渐增强的顺序排列的是
A. Na、K、Rb B. F、Cl、Br
C. Mg2+、Al2+、Zn2+ D. Cl-、Br-、I-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com