
某课外实验小组欲探究铝和铜的金属性(原子失电子能力)强弱,同学们提出了如下实验方案:
A.比较铝和铜的硬度和熔点;
B.比较二者在稀硫酸中的表现;
C.用铝片、铜片、硫酸铝溶液、硫酸铜溶液,比较二者的活动性;
D.分别做铝片、铜片与NaOH溶液反应的实验;
E.分别做Al(OH)3和Cu(OH)2与NaOH溶液反应的实验;
F.比较Al(OH)3和Cu(OH)2的热稳定性;
G.将铝片、铜片用导线连接后共同浸入浓硝酸中,接入电流计,观察电流方向。
(1)你认为上述方案中能达到实验目的有 ;
(2)上述7个方案中除G外,可以设计成电池反应的还有 ;
(3)写出D方案中反应的化学方程式 ;
(4)G方案中,因为铝片在浓硝酸中发生 ,故电池的负极是 ;写出该电池总反应的离子方程式 。
科目:高中化学 来源: 题型:阅读理解
 某课外兴趣小组欲探究铝与盐酸反应的能量变化以及影响化学反应速率的因素.做如下实验,请填写下列空白:
某课外兴趣小组欲探究铝与盐酸反应的能量变化以及影响化学反应速率的因素.做如下实验,请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:山东省日照一中2011-2012学年高一下学期模块笔试(学段调研)化学试题 题型:058
某课外实验小组欲探究铝和铜的金属性(原子失电子能力)强弱,同学们提出了如下实验方案:
A.比较铝和铜的硬度和熔点;
B.比较二者在稀硫酸中的表现;
C.用铝片、铜片、硫酸铝溶液、硫酸铜溶液,比较二者的活动性;
D.分别做铝片、铜片与NaOH溶液反应的实验;
E.分别做Al(OH)3和Cu(OH)2与NaOH溶液反应的实验;
F.比较Al(OH)3和Cu(OH)2的热稳定性;
G.将铝片、铜片用导线连接后共同浸入浓硝酸中,接入电流计,观察电流方向.
(1)你认为上述方案中能达到实验目的有________;
(2)上述7个方案中除G外,可以设计成电池反应的还有________;
(3)写出D方案中反应的化学方程式________;
(4)G方案中,因为铝片在浓硝酸中发生________,故电池的负极是________;写出该电池总反应的离子方程式________.
查看答案和解析>>
科目:高中化学 来源: 题型:
(14分)某课外兴趣小组欲探究铝与盐酸的反应实验中反应速率与哪些因素有关。请填写下列空白:
(1)实验反应原理: 。
(2)实验用品:试管(普通试管和具支试管各一支)、镊子、乳胶管、玻璃导管、
水槽、胶头滴管、温度计;稀盐酸(4mol/L)、铝条(片)、水。
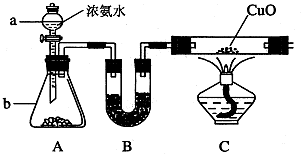
(3)实验装置 (图中铁架台等夹持仪器略去)
(4)实验方法
①按如图所示连接好实验仪器,检查装置的气密性,具体操作方法是: 。
②取3块铝条加入到试管中,操作方法是 。
③在盛有铝条的试管中,加入2mL稀盐酸。
④测量试管中溶液的温度。
⑤收集反应产生的氢气。
(5)数据处理及问题讨论
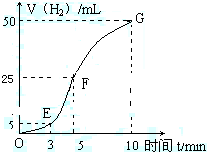
①实验结束后,课外兴趣小组成员将产生氢气的体积与时间作了如图。
②试判断OE、EF、FG段所收集气体的多少。
OE: ;EF: ;FG: 。
写出这三个时间段内产生氢气的速率大小比较(用OE、EF、FG表示)。速率大小比较: ,在三个时间段反应平均速率变化的原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com