

| 序号 | 甲试管里发生反应的物质 | U形管里红墨水液面 |
| ① | 氧化钙与水 | 左低右高 |
| ② | 氢氧化钡晶体与氯化铵晶体(充分搅拌) | ? |
| ③ | 铝片与烧碱溶液 | 左低右高 |
| ④ | 铜与浓硝酸 | 左低右高 |
分析 (1)温度计的温度由20℃逐渐升至75℃,说明铝片与盐酸反应为放热反应,离子方程式为:2Al+6H+═2Al3++3H2;
(2)反应完全后,热量向空气中传递,烧杯里物质的温度降低;
(3)反应放热,温度升高,蜡烛熔化了;
(4)若放热反应,则U形管内气体膨胀,压强增大,U形管里红墨水液面出现左低右高的现象;
(5)中出现了液面左低右高的现象,故物质发生的反应都是放热反应,如果放置,温度回复到室温,可观察到U形管里的液面左右相平;
(6)氢氧化钡晶体与氯化铵晶体(充分搅拌)反应为典型的吸热反应.
解答 解:(1)温度计的温度由20℃逐渐升至75℃,说明铝片与盐酸反应为放热反应,离子方程式为:2Al+6H+═2Al3++3H2↑,故答案为:放热;2Al+6H+═2Al3++3H2↑;
(2)方案一中,温度升至最大值后又下降的原因是反应完全后,热量向空气中传递,烧杯里物质的温度降低,故答案为:反应完全后,热量向空气中传递,烧杯里物质的温度降低;
(3)方案二中,小木片脱落的原因是反应放热,温度升高,蜡烛熔化了,故答案为:蜡烛熔化;氢氧化钠与硫酸的反应放热;
(4)如果甲试管里发生的反应是放热反应,则U形管内气体膨胀,压强增大,U形管里红墨水液面出现左低右高的现象,故答案为:低于;
(5)由方案三的现象得出结论:①③④组中出现了液面左低右高的现象,故物质发生的反应都是放热反应,如果放置,温度回复到室温,可观察到U形管里的液面左右相平,故答案为:放热;红墨水液面左右相平;
(6)氢氧化钡晶体与氯化铵晶体(充分搅拌)反应为典型的吸热反应,故红墨水液面左高右低,反应物总能量低于生成物总能量,故答案为:红墨水液面左高右低;小于.
点评 本题考查吸热反应和放热反应,把握实验操作的规范性、实验细节和实验原理为解答的关键,注意方案的合理性、评价性、操作性分析,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 第二周期 IVA族 | B. | 第三周期 IV A族 | C. | 第三周期 VI A族 | D. | 第二周期VI A族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
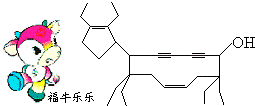
| A. | 牛式二烯炔醇含有4种官能团 | |
| B. | 牛式二烯炔醇不能使酸性KMnO4溶液褪色 | |
| C. | 1 mol牛式二烯炔醇最多可跟4mol Br2发生加成反应 | |
| D. | 该有机物的化学式为C29H44O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
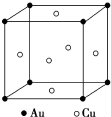 金和铜可以形成多种金属化合物,其中一种晶体的结构如图所示(为面心立方体结构).
金和铜可以形成多种金属化合物,其中一种晶体的结构如图所示(为面心立方体结构).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制取乙烯时浓硫酸是催化剂和吸水剂 | |
| B. | 硝基苯制备时浓硫酸作催化剂和脱水剂 | |
| C. | 实验室制备乙烯、硝基苯、苯磺酸时均使用到温度计,且水银球在反应混合物液面以下 | |
| D. | 水浴加热的优点是可以受热均匀且便于控制温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Pb为正极被氧化 | B. | SO42-只向PbO2处移动 | ||
| C. | Pb电极质量减少 | D. | 电解质溶液的pH不断增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 17gNH3中含有的质子数为10NA | |
| B. | 标准状况下,22.4LCl2与56gFe反应生成FeCl2分子的数目为NA | |
| C. | 7.0g丁烯含有C-H键的数目为NA | |
| D. | 常温下,1.0LpH=1的H2SO4溶液中,由水电离出的0H-的数目为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com