
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
在一恒定的容器中充入2 mol X和1 mol Y发生反应:2X(g)+Y(g) nZ(g)达到平衡后,Z的体积分数为a%;若维持容器的容积和温度不变,按起始物质的量X为0.6 mol,Y为0.3 mol,Z为1.4 mol充入容器中,达到平衡后,Z的体积分数仍为a%,则n的值为( )。
nZ(g)达到平衡后,Z的体积分数为a%;若维持容器的容积和温度不变,按起始物质的量X为0.6 mol,Y为0.3 mol,Z为1.4 mol充入容器中,达到平衡后,Z的体积分数仍为a%,则n的值为( )。
A.可能为2,也可能为3 B.只能为3
C.只能为2 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)中和热的测定实验(如图)。
①量取反应物时,取50 mL 0.50 mol/L的盐酸,还应
加入的试剂是 (填序号)。
A.50 mL 0.50 mol/LNaOH溶液
B.50 mL 0. 55 mol/LNaOH溶液
C.1.0 g NaOH固体
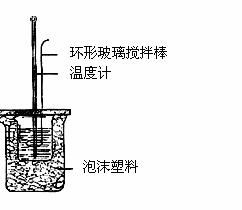
②在实验过程中,该同学需要测定并记录的实验数据有 (填序号)。
A.盐酸的浓度 B.盐酸的温度 C.氢氧化钠溶液的浓度
D.氢氧化钠溶液的温度 E.水的比热容 F.反应后混合溶液的最高温度
③若用50 mL 0.50 mol/L的醋酸溶液代替上述盐酸测定中和热,所得数据 (填“偏大”或“偏小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
NA表示阿伏加德罗常数,下列说法中不正确的是
A.KIO3+6HI=KI+3H2O+3I2 ,生成3mol I2转移电子的总数为5NA
B.标准状况下,5.6 L氧气中含有O的总数为0.5NA
C.25℃时,pH=13的Ba(OH)2溶液1.0L中含有OH-总数为0.1NA
D.20 g重水(D2O)中所含电子总数为8NA
查看答案和解析>>
科目:高中化学 来源: 题型:
利用I2O5可消除CO污染或定量测定CO,反应为:
5CO(g)+I2O5(s)
 5CO2(g)+I2(s);ΔH 1
5CO2(g)+I2(s);ΔH 1
(1)已知:2CO(g)+O2(g)
 2CO2(g);ΔH 2
2CO2(g);ΔH 2
2I2(s)+5O2(g)
 2I2O5(s);ΔH 3
2I2O5(s);ΔH 3
则ΔH 1= (用含ΔH 2和ΔH 3的代数式表示)。
 (2)不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入2molCO,测得CO2的体积分数φ(CO2)随时间t变化曲线如右图。请回答:
(2)不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入2molCO,测得CO2的体积分数φ(CO2)随时间t变化曲线如右图。请回答:
①从反应开始至a点时的反应速率为v(CO)= ,b点时化学平衡常数Kb= 。
②d点时,温度不变,若将容器体积压缩至原来的一半,请在图中补充画出CO2体积分数的变化曲线。
③下列说法正确的是 。(填字母序号)
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的平均相对分子质量相等
C.增加I2O5的投料量有利于提高CO的转化率
D.b点和d点的化学平衡常数:Kb<Kd
(3)将500mL(标准状况)含有CO的某气体样品通过盛有足量I2O5的干燥管,170℃下充分反应,用水—乙醇液充分溶解产物I2,定容到100mL。取25.00mL,用0.0100mol·L-1 Na2S2O3标准溶液滴定,消耗标准溶液20.00mL,则样品气中CO的体积分数为 。(已知:气体样品中其他成分与I2O5不反应;2Na2S2O3+I2=2NaI+Na2S4O6)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验不能达到实验目的的是
A.用结晶法提纯混有少量氯化钾的硝酸钾
B.用KSCN检验溶液中Fe3+的存在
C.用湿润的淀粉碘化钾试纸检验氯气
D. 用酒精萃取碘水中的碘
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法中不正确的是
A、共价化合物一定有极性共价键,可能含有离子键
B、离子化合物一定含离子键,可能含非极性共价键
C、元素周期表中从ⅢB族到ⅡB族10个纵行的元素都是金属元素
D、短周期中含有五种金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格:
(1)在这10种元素中,非金属性最强的是___________(填序号);
(2)元素②⑧⑨以原子个数比1:1:1形成的化合物的结构式为______________,元素②与⑨形成的18e-化合物的电子式____________________;
(3)②、⑨、⑩三种元素形成的化合物M中原子个数比为3:4:2,电子总数为42,M中含有的化学键类型有___________________________;
(4)比较元素⑦⑧形成的气态氢化物的稳定性:____>____(用化学式表示)
(5)元素⑤的氧化物与氢氧化钠溶液反应的离子方程式______________________。
(6)元素④和③形成的化合物属于 化合物,用电子式表示其形成过程 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com