
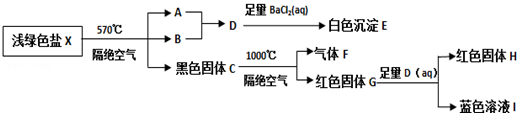
���� dz��ɫ��X��570�桢�����������������ȷֽ�Ϊ��������ԭ��Ӧ���õ�A��B�ͺ�ɫ����C��������B��Һ̬��1��B���Ӻ���10�����ӣ�BΪˮ��A��ˮ��Ӧ���ɵ�D�ܺ��Ȼ�����Ӧ���ɰ�ɫ����E��Eֻ��Ϊ���ᱵ��23.3g��ɫ����E�����ʵ���Ϊn=$\frac{m}{M}$=$\frac{23.3g}{233g/mol}$=0.1mol����ɫ����C����Ϊ����������������ͭ��̼�ȣ���ɫ����C����������1000�淴Ӧ��������F�ͺ�ɫ����G��G�ܺ����ᷴӦ���ɺ�ɫ�������ɫ��ҺӦΪ������ͭ��������Һ�е��绯��Ӧ�����Ժ�ɫ����GΪ������ͭ������FΪ��������ɫHΪͭ����ɫ��ҺIΪ����ͭ��
���ƿɵã�һ������dz��ɫ��X��n��S��=0.1mol��28.8g��ɫ����GΪ������ͭ��n��Cu2O��=$\frac{28.8g}{144g/mol}$=0.2mol��12.8g��ɫ����H��n��Cu��=0.2mol��dz��ɫ��X��n��Cu��=0.4mol��n��CuO��=0.4mol��dz��ɫ��X��570�桢�����������������ȷֽ�Ϊ��������ԭ��Ӧ��n��S��=0.1mol������n��CuO����n��SO3��=1��4��dz��ɫ��X����������Ԫ�أ������ᾧˮ���軯ѧʽΪ��Cu4��OH��mSO4��Cu4��OH��mSO4$\frac{\underline{\;\;��\;\;}}{\;}$4CuO+SO3��+$\frac{m}{2}$H2O����������Ԫ���غ�ã�m=6������M��X����908g•mol-1����÷�Ӧ����Ϊ��X�ڸ���������570���¶��¼���Cu4��OH��6SO4$\frac{\underline{\;\;��\;\;}}{\;}$4CuO+SO3��+3H2O����A��B��ӦSO3+H2O=H2SO4�������������Ȼ�����Ӧ��H2SO4+BaCl2=BaSO4��+2HCl����ɫ����EΪBaSO4����ɫ����CΪ����ͭ����1000�淴Ӧ��������FΪ��������ɫ����GΪ������ͭ4CuO$\frac{\underline{\;1000��\;}}{\;}$2Cu2O+O2����G������ͭ�����ᷢ���绯��Ӧ��Cu2O+H2SO4=CuSO4+Cu+H2O����ɫHΪͭ����ɫ��ҺIΪ����ͭ���ݴ˷������
��� �⣺��1��BΪˮ��ˮ�ǹ��ۻ������ԭ�Ӻ���ԭ��֮���Թ��ۼ���ϣ������ʽΪ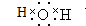 ��
��
�ʴ�Ϊ��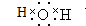 ��
��
��2����ɫ����GΪ������ͭ��Cu2O��+1�۵�ͭ������������ϡ���ᱻ��ԭ��һ����������ӦΪ��3Cu2O+14H++2NO3-�T6Cu2++2NO��+7H2O��
�ʴ�Ϊ��3Cu2O+14H++2NO3-�T6Cu2++2NO��+7H2O��
��3��dz��ɫ��X��n��Cu��=0.4mol��n��S��=0.1mol��n��CuO����n��SO3��=1��4����������Ԫ�أ������ᾧˮ���軯ѧʽΪ��Cu4��OH��mSO4��Cu4��OH��mSO4$\frac{\underline{\;\;��\;\;}}{\;}$4CuO+SO3��+$\frac{m}{2}$H2O����������Ԫ���غ�ã�m=6������M��X����908g•mol-1���ʴ�Ϊ��Cu4��OH��6SO4��
���� ���⿼����������ɵ��ƶϣ��漰���ӵļ��顢���ʵ����ʵ�֪ʶ�㣬��ϤԪ�ػ���������ʡ�֪������ͼ��ÿһ�������ķ�Ӧ����Ӧ�����ǽⱾ��ؼ�����Ŀ�Ѷ��еȣ�


 ��������ϵ�д�
��������ϵ�д� ��ӡ�Ļ���ʱ����ϵ�д�
��ӡ�Ļ���ʱ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��̬�⻯����ȶ��ԣ�X��Z��W | |
| B�� | Y�������Ӱ뾶��W�������Ӱ뾶С | |
| C�� | X��Z��W����������Ӧˮ�������Ե�ǿ��˳��ΪX��Z��W | |
| D�� | �����£���YԪ�ص����γɵ�ˮ��Һ��pH��7 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ba��OH��2�TBa2++2 OH- | B�� | H3PO4 3?H++PO43- | ||
| C�� | HI=H++I- | D�� | NH3•H2O?NH4++OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ�����м����������������������ĵ���̶� | |
| B�� | 25��ʱ������������ʵ���Ũ�ȵ������백ˮ��Ϻ���ҺpH=7 | |
| C�� | 25��ʱ��0.1 mol•L-1��������Һ�ȵ�Ũ�ȵ�������Һ�ĵ��������� | |
| D�� | PH=2����HA��Һ��PH=12�ļ�BOH��Һ�������Ϻ�������Һ�����ԣ�֤��HAΪǿ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH4+��Al3+��SO42-��NO3- | B�� | K+��Na+��SO42-��Ba2+ | ||
| C�� | K+��MnO4-��NH4+��Cl- | D�� | Ca2+��K+��HCO3-��NO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �屽��ˮ | B�� | 1��2-����������� | ||
| C�� | �ƾ���ˮ | D�� | ������ͱ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com