
在一定温度下,冰醋酸加水稀释过程中,溶液的导电能力如下图所示,请回答:

(1)“O”点导电能力为0的理由是 。
(2)A、B、C三点溶液c(H+)由小到大的顺序为 。
(3)若使C点溶液中c(CH3COO-)增大的同时溶液的c(H+)减小,可采取的措施是:
① ;② ;③ 。
(4)经实验测得C点处:c(CH3COOH)=0.1 mol·L-1,c(CH3COO-)=0.01 mol·L-1,则该条件下CH3COOH的电离常数Ka= 。
(1)CH3COOH是共价化合物,无水不电离,也就无自由移动的离子,所以不导电
(2)C<A<B
(3)加活泼金属(如Mg) 加碱性氧化性(如Na2O) 加碱(如NaOH) 加某些盐(如Na2CO3) 加醋酸盐(如CH3COONa)(任选三种)
(4)1×10-3
【解析】
试题分析: (1)CH3COOH是一种共价化合物,是弱电解质,共价化合物只有在水溶液里才能电离导电。“O”点不导电说明此时CH3COOH未电离,说明此时无水,不电离,不存在自由移动的离子。
(2)c(H+)越小,导电能力越弱;c(H+)越大,导电能力越强。故c(H+)由小到大的顺序为C<A<B。
(3)欲使c(CH3COO-)增大,可以使平衡右移,即消耗c(H+)的办法,此时可考虑酸的五大通性,其中适合的有加金属、金属氧化物、碱、某些盐;也可以使平衡逆向移动,此时只能加醋酸盐。
(4)由CH3COOH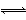 CH3COO-+H+,可知c(H+)=c(CH3COO-)=0.01 mol·L-1,则Ka==1×10-3。
CH3COO-+H+,可知c(H+)=c(CH3COO-)=0.01 mol·L-1,则Ka==1×10-3。
考点:弱电解质的电离


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)4.2.2燃料电池试卷(解析版) 题型:选择题
美国加州Miramar海军航空站安装了一台250 kW的MCFC型燃料电池,该电池可同时供应电和水蒸气,其工作温度为600~700 ℃,所用燃料为H2,电解质为熔融的K2CO3。该电池的总反应为2H2+O2 2H2O,负极反应为H2+C-2e-
2H2O,负极反应为H2+C-2e- H2O+CO2。则下列推断中正确的是( )
H2O+CO2。则下列推断中正确的是( )
A.正极反应:4OH--4e- 2H2O+O2↑
2H2O+O2↑
B.当电池生成1 mol H2O时,转移4 mol电子
C.放电时C向负极移动
D.放电时C向正极移动
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.2水的电离溶液的酸碱性(解析版) 题型:选择题
25 ℃时,水的电离达到平衡:H2O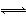 H++OH- ΔH>0,下列叙述正确的是( )
H++OH- ΔH>0,下列叙述正确的是( )
A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变
C.向水中加入少量固体NaOH,平衡逆向移动,c(H+)降低,KW减小
D.将水加热,KW增大,pH不变
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.2.3 酸碱中和滴定(解析版) 题型:选择题
下列有关滴定操作的顺序正确的是( )
①用标准溶液润洗滴定管 ②往滴定管内注入标准溶液 ③检查滴定管是否漏水 ④滴定 ⑤洗涤
A.⑤①②③④B.③⑤①②④ C.⑤②③①④ D.②①③⑤④
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.2.2 pH的计算试卷(解析版) 题型:选择题
常温下,将0.1 mol·L-1氢氧化钠溶液与0.06 mol·L-1硫酸溶液等体积混合,该混合溶液的pH等于( )
A.1.7B.2.0 C.12.0 D.12.4
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)3.1弱电解质的电离试卷(解析版) 题型:选择题
把1 L 0.1 mol·L-1醋酸溶液用蒸馏水稀释到10 L,下列叙述正确的是( )
A.c(CH3COOH)变为原来的
B.c(H+)变为原来的
C.的比值增大
D.溶液的导电性增强
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步课时练(人教选修4)2.3.3化学平衡常数试卷(解析版) 题型:填空题
高炉炼铁中发生的基本反应之一如下:
FeO(s)+CO(g) Fe(s)+CO2(g) ΔH>0,其平衡常数表达式为K= ,又知1 100 ℃时,K=0.28。
Fe(s)+CO2(g) ΔH>0,其平衡常数表达式为K= ,又知1 100 ℃时,K=0.28。
(1)温度升高,化学平衡移动后达到新的平衡,平衡常数 。(填“变大”“变小”或“不变”)
(2)1 100 ℃时测得高炉中c(CO2)=0.013 mol·L-1,c(CO)=0.05 mol·L-1,在这种情况下,该反应是否处于化学平衡状态: (填“是”或“否”),此时,化学反应速率是v(正) v(逆)(填“大于”“小于”或“等于”),其原因 。
查看答案和解析>>
科目:高中化学 来源:2015安徽望江中学同步练(人教选修4)2.3化学平衡状态的建立及标志(解析版) 题型:填空题
在2 L密闭容器内,800 ℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
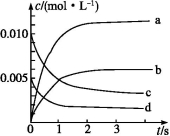
(1)上图表示NO2的浓度变化的曲线是 。用O2表示从0~2 s内该反应的平衡速率v= 。
(2)能说明该反应已达到平衡状态的是 。
a.v(NO2)=2v(O2) b.容器内压强保持不变c.v逆(NO)=2v正(O2) d.容器内密度保持不变
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学钠及其化合物主要性质(解析版) 题型:选择题
下列类比关系正确的是
A.钠与氧气在不同条件下反应会生成两种不同的氧化物,则Li与氧气反应也能生成Li2O或Li2O2
B.Na2O2与CO2反应生成Na2CO3和O2,则Na2O2与SO2反应可生成Na2SO3和O2
C.Fe与Cl2反应生成FeCl3,则Fe与I2反应可生成FeI3
D.Al与Fe2O3能发生铝热反应,则Al与MnO2也能发生铝热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com