
 图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:| V×1000mL×1.19g?cm-3×36.5% |
| 36.5mol/L |
| 11.9Vmol |
| VL |
| 103ρw |
| M |


 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:
| A、过量铁与浓硫酸加热反应可以得到氢气 |
| B、硅酸盐NaAlSiO4?nH2O可改写成氧化物形式为:Na2O?Al2O3?2SiO2?2nH2O |
| C、某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为水中溶解了较多的CO2 |
| D、Al65Cu23Fe12是一种拟晶,具有合金的优良物理性能,其硬度比金属A1、Cu、Fe都大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
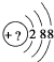 (1)该微粒是中性微粒,这种微粒的符号是
(1)该微粒是中性微粒,这种微粒的符号是查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 | B、3 | C、4 | D、5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应中NF3是氧化剂,H2O是还原剂 |
| B、反应中被氧化与被还原的原子物质的量之比为2:1 |
| C、若反应中生成0.2 mol HNO3,则反应共转移0.2 mol e- |
| D、NF3在潮湿空气中泄漏会产生白雾、红棕色气体等现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸钡、碳酸氢钠、氢氧化铝均可作为抗酸药物使用 |
| B、人体内的蛋白质不断分解,最终生成水和二氧化碳排出体外 |
| C、工业生产玻璃和水泥,均需要用纯碱为原料 |
| D、“地沟油”的主要成分是油脂,其组成与汽油、煤油不相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
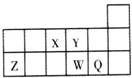
| A、原子半径Y<Z<W |
| B、元素Y的最高正化合价比元素X的最高正化合价高 |
| C、元素W的最高价氧化物对应的水化物的酸性比Q的弱 |
| D、元素X的气态氢化物的稳定性大于元素Y的气态氢化物的稳定性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com