
有pH=12的NaOH溶液100mL.如果将其pH降为11,那么:(忽略混合时溶液体积的变化)
(1)若用蒸馏水应加入 mL
(2)若用pH=10的NaOH溶液应加入 mL
(3)若用pH=2的盐酸溶液应加入 mL
(4)若用0.01mol∙L﹣1的醋酸应加入的范围是 .
考点:
pH的简单计算.
分析:
(1)先根据溶液的pH计算氢氧根离子浓度,再根据C1V1=C2(V1+V2)计算加入的水体积;
(2)先根据溶液的pH计算氢氧根离子浓度,再根据C1V1+C2V2=C3(V1+V2)计算加入的氢氧化钠溶液体积;
(3)先计算混合溶液中氢氧根离子浓度,再根据C(OH﹣)= ;
;
(4)假设为强酸,计算需要加入酸的体积,实际上醋酸是弱酸,加入的体积应该稍微大于此值.
解答:
解:(1)pH=12 的NaOH溶液中氢氧根离子浓度是0.01mol/L,pH=11的氢氧化钠溶液中氢氧根离子浓度是0.001mol/L,设加入水的体积是V2,C1V1=C2(V1+V2)=0.01mol/L×0.1L=(0.1+V2)L,V2=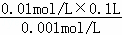 =0.9L=900mL,故答案为:900;
=0.9L=900mL,故答案为:900;
(2)pH=12 的NaOH溶液中氢氧根离子浓度是0.01mol/L,pH=11的氢氧化钠溶液中氢氧根离子浓度是0.001mol/L,pH=10的氢氧化钠溶液中氢氧根离子浓度是0.0001mol/L,
设加入pH=10的NaOH溶液体积是V2,C1V1+C2V2=C3(V1+V2)=0.01mol/L×0.1L+0.0001mol/L×V2=0.001mol/L(0.1+V2),V2=1L=1000mL,故答案为:1000;
(3)pH=2的HCl溶液中氢离子浓度是0.01mol/L,设加入盐酸的体积是V,C(OH﹣)= ,
,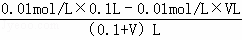 =0.001mol/L,v=81.8mL,
=0.001mol/L,v=81.8mL,
故答案为:81.8;
(4)假设加入醋酸是强酸,根据(3)知,加入的醋酸应该是81.8mL,但CH3COOH为弱酸,加入81.8 mL后溶液pH>11,故加入的CH3COOH应大于81.8 mL,
故答案为:V>81.8 mL.
点评:
本题考查溶液pH的简单计算,难点(4)题计算醋酸溶液的体积,利用假设法进行分析解答即可,难度较大.


科目:高中化学 来源: 题型:
已知450℃时,反应H2(g)+I2(g)⇌2HI(g)的K=50,由此推测在450℃时,反应 2HI(g)⇌H2(g)+I2(g)的化学平衡常数为( )
|
| A. | 50 | B. | 0.02 | C. | 100 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某酸碱指示剂是一种有机弱酸,其在水溶液中的电离平衡与其呈颜色有关:HIn(红色)⇌H++In﹣(黄色),若向含此指示剂的溶液中加入盐酸,溶液呈 色.若向此溶液中加入氢氧钠,溶液呈 色.
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下,某溶液中由水电离出的c(OH﹣)=10﹣5 mol•L﹣1,则其溶质可能是( )
|
| A. | CH3COOH | B. | H2SO4 | C. | NaOH | D. | Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
pH=2的A、B两种酸溶液各1mL,分别加水稀释到1L(其pH与溶液体积V的关系如图所示),下列说法正确的是( )
①a=5时,A是强酸,B是弱酸;
②若A、B都是弱酸,则5>a>2;
③稀释后,A酸溶液的酸性比B酸溶液强;
④A、B两种酸溶液的物质的量浓度一定相等.

|
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列过程或现象与盐类水解无关的是( )
|
| A. | 热的Na2CO3溶液可以除去油污 |
|
| B. | ZnCl2和NH4Cl溶液可作金属焊接中的除锈剂 |
|
| C. | 用食醋除水垢 |
|
| D. | 将AlCl3溶液加热蒸干、灼烧,最后得到的固体时Al2O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,反应SO2(g)+ O2(g)⇌SO3(g)的平衡常数K1=50,在同一温度下,反应2SO3(g)⇌2SO2(g)+O2(g)的平衡常数K2的值为( )
O2(g)⇌SO3(g)的平衡常数K1=50,在同一温度下,反应2SO3(g)⇌2SO2(g)+O2(g)的平衡常数K2的值为( )
|
| A. | 2500 | B. | 100 | C. | 4×10﹣4 | D. | 2×10﹣2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,甲池的总反应式O2+N2H4 2H2O+N2。有关该装置工作时,说法正确的是
2H2O+N2。有关该装置工作时,说法正确的是
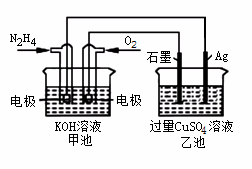
A.甲池中,负极反应为N2H4-4e- 4H++N2
4H++N2
B.甲池溶液pH保持不变,乙池溶液pH减小
C.甲池中消耗2.24LO2,此时乙池中理论上最多产生12.8g固体
D.反应一段时间后,向乙池中加一定量CuO固体,能使CuSO4溶液恢复到原浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
在25℃时将pH=11 的NaOH 溶液与pH=3 的CH3COOH溶掖等体积混合后,下列关系式中正确的是( )
|
| A. | c(Na+)=c(CH3COO﹣)+c(CH3COOH) | B. | c(H+)=c(CH3COO﹣)+c(OH﹣) |
|
| C. | c(Na+)>c(CH3COO﹣)>c(OH﹣)>c(H+) | D. | c(CH3COO﹣)>c(Na+)>c(H+)>c(OH﹣) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com