
【题目】功能高分子P的合成路线如下:
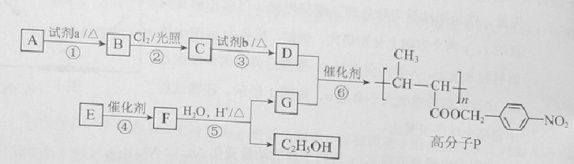
(1)A的分子式是C7H8,其结构简式是___________________。
(2)试剂a是_______________。
(3)反应③的化学方程式:_______________。
(4)E的分子式是C6H10O2。E中含有的官能团:_______________。
(5)反应④的反应类型是_______________。
(6)反应⑤的化学方程式:_______________。
(5)已知:2CH3CHO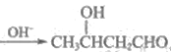 。
。
以乙烯为起始原料,选用必要的无机试剂合成E,写出合成路线(用结构简式表示有机物),用箭头表示转化关系,箭头上注明试剂和反应条件)。
【答案】(1) (2)浓硫酸和浓硝酸 (3)
(2)浓硫酸和浓硝酸 (3)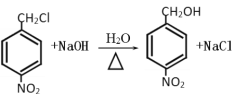
(4)碳碳双键、酯基 (5)加聚反应
(6)
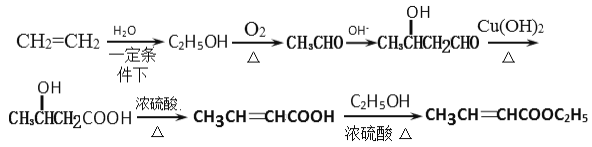
(7)
【解析】
试题分析:根据高分子P的结构和A的分子式为C7H8,可以推出,D为对硝基苯甲醇,因此A应该为甲苯,B为对硝基甲苯,B与氯气发生取代反应生成C为一氯甲基对硝基苯,结构简式为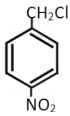 。根据D和P的结构简式可知D和G发生酯化反应生成P,因此G的结构简式为
。根据D和P的结构简式可知D和G发生酯化反应生成P,因此G的结构简式为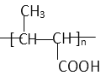 。F水解生成G和乙醇,因此F的结构简式为
。F水解生成G和乙醇,因此F的结构简式为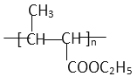 。E在催化剂的作用下转化为F,这说明反应④是碳碳双键的加聚反应,因此E的结构简式为CH3CH=CHCOOC2H5。
。E在催化剂的作用下转化为F,这说明反应④是碳碳双键的加聚反应,因此E的结构简式为CH3CH=CHCOOC2H5。
(1)根据以上分析可知A的结构式为 ;
;
(2)甲苯和硝酸在浓硫酸催化作用下生成对硝基苯,所以试剂a为浓硫酸和浓硝酸;
(3)反应③是一氯甲基对硝基苯在氢氧化钠的水溶液中发生取代反应生成对硝基苯甲醇,反应的化学方程式为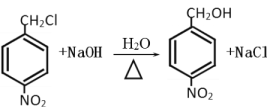 ;
;
(4)根据E的结构式为CH3CH=CHCOOC2H5可知所含官能团有碳碳双键、酯基;
(5)F应该是E发生加聚反应生成的一个高分子化合物,所以反应④是加聚反应;
(6)反应⑤的化学方程式为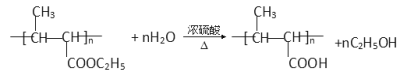 。
。
(7)乙烯和水可以直接加成生成乙醇,乙醇氧化生成乙醛,乙醛发生已知条件中的反应既可以使碳链增长,由于碳碳双键易被氧化,因此首先发生消去反应,然后再氧化醛基为羧基,羧酸和乙醇发生酯化反应,即可得物质E,合成路线为:


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案科目:高中化学 来源: 题型:
【题目】以NaCl、CO2、NH3为原料发生反应,制得NaHCO3和NH4Cl是“侯氏制碱法”的重要步骤。相关物质的溶解度曲线如图所示。下列说法不正确的是
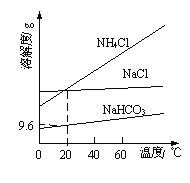
A.将NaHCO3加热分解可得纯碱
B.常温下碳酸氢钠的溶解度大于碳酸钠
C.采用蒸发结晶从溶液中分离出NaHCO3
D.20℃时,NaHCO3饱和溶液的物质的量浓度约为1.1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡及其化合物在生产、生活中有着重要的用途。已知:Sn的熔点为231℃;Sn2+易水解、易被氧化;SnCl4极易水解、熔点为-33 ℃、沸点为114 ℃。请按要求回答下列相关问题:
(1)锡在周期表中的位置为_____________.
(2)用于镀锡工业的硫酸亚锡(SnSO4)的制备步骤如下:
I.SnCl2加入盐酸和Sn 粉
II.分离滤渣和滤液
Ⅲ.滤液用NaHCO3调节pH至6~7 得混合物(含SnO)
Ⅳ.从混合物中分离得SnO
V.SnO和稀硫酸最终得SnSO4晶体
①步骤Ⅰ加入Sn粉的作用: _________________及调节溶液pH。
②步骤Ⅱ用到的玻璃仪器有烧杯、_______________、______________。
③步骤Ⅲ生成SnO的离子方程式:_________________________。
④步骤Ⅳ中检验SnO是否洗涤干净的操作是_____________________,证明已洗净。
⑤步骤Ⅴ操作依次为 _____________、____________、过滤、洗涤、低温干燥。
(3)SnCl4蒸气遇氨及水汽呈浓烟状,因而可制作烟幕弹,其反应的化学方程式为__________________。
实验室欲用下图装置制备少量SnCl4(夹持装置略),该装置存在明显缺陷,改进方法是__________。
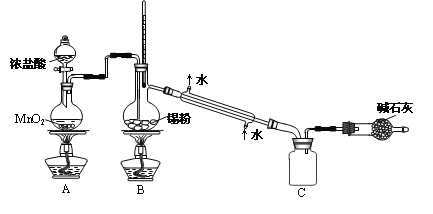
(4)利用改进后的装置进行实验,当开始装置C中收集到有SnCl4时即可熄灭B处酒精灯,反应仍可持续进行的理由是_________________。
(5)用于微电子器件生产的锡粉纯度测定:
①取2.38g试样溶于较浓硫酸中(杂质不参与反应),使Sn完全转化为Sn2+;
②加入过量的Fe2(SO4)3;
③用0.1000mol/LK2Cr2O7溶液滴定,消耗20.00mL。步骤②中加入Fe2(SO4)3的作用是:__________;此锡粉样品中锡的质量分数:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.下表为周期表的一部分,其中的编号代表对应的元素。

(1)写出上表中元素I的价层电子排布图 。元素C、D、E、F的第一电离能由大到小的顺序是 (用元素符号表示)。
(2)元素A分别与C、D、E形成最简单的常见化合物分子甲、乙和丙。下列有关叙述不正确的有( )
A.甲、乙和丙分子的空间构型分别为正四面体形、三角锥形、V形
B.甲、乙和丙分子中,中心原子均采取sp3的杂化方式
C.三种分子中键角由大到小的顺序是丙>乙>甲
D.甲、乙和丙分子均为由极性键构成的极性分子
(3)由元素J、C、E组成一种化学式为J(CE)的配位化合物,该物质常温下呈液态,熔点为一20.5℃,沸点为103℃,易溶于非极性溶剂。据此可判断:该化合物的晶体中存在的作用力有( )
A.离子键
B.极性键
C.非极性键
D.范德华力
E.氢键
F.配位键
Ⅱ.(1) BCl3中B原子的杂化方式为 。第一电离能介于B、N之间的第二周期元素有 种。写出与BCl3结构相同的一种等电子体 (写离子)。
(2)科学家测得胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下:
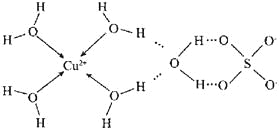
①胆矾的化学式用配合物的形式表示为的 ;
②胆矾中SO42-的空间构型为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 二氧化硅可制玻璃、单质硅、光导纤维;
B. 食盐、糖、醋可作调味剂,不可作食品防腐剂;
C. 金属腐蚀的本质是金属原子失电子被氧化的过程;
D. 大量服用阿司匹林会出现水杨酸中毒症,可静脉滴注NaHCO3溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有学生在实验室中向盛有10mL饱和氯化铁溶液的试管里投入足量铝片,观察到如下现象:
①黄色溶液很快变成红褐色,过一会儿溶液中有红褐色沉淀生成。
②铝片表面立刻有少量黑色物质析出,黑色物质能被磁铁吸起。
③混合液温度升高甚至发烫,产生无色气泡,且产生气泡速率明显加快,铝片上下翻滚。
(1)产生的红褐色沉淀是______________,无色气泡的成分是___________。
(2)生成红褐色沉淀的原因是_____________________________。
(3)写出生成气泡速率明显加快的两个原因____________、_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高血脂严重影响人体健康,化合物E是一种临床治疗高血脂症的药物。E的合成路线如下(部分反应条件和试剂略):
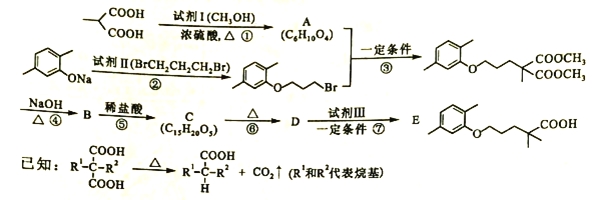
请回答下列问题:
(1)试剂I的名称是____a____,试剂II中官能团的名称是____b___,第② 步的反应类型是____c___。
(2)第①步反应的化学方程式是_____________。
(3)第⑥步反应的化学方程式是_____________。
(4)第⑦步反应中,试剂Ⅲ为单碘代烷烃,其结构简式是_________ 。
(5)C的同分异构体在酸性条件下水解,生成X、Y和CH3(CH2)4OH。若X含有羧基和苯环,且X和Y的核磁共振氢谱都只有两种类型的吸收峰,则X与Y发生缩聚反应所得缩聚物的结构简式是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烷和丙烷的混合气体完全燃烧后,先将产物通过浓硫酸,充分吸收后浓硫酸增重3.06g;然后通过过氧化钠固体,充分反应后固体增重3.36g.混合气体中乙烷和丙烷的体积比为( )
A.1:1 B.2:3 C.3:2 D.3:5
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com