
| 步骤一:取少量制品于试管中,加少量蒸馏水,振荡,溶解。往试管中加入 振荡,观察 | 现象:溶液中产生大量白色沉淀; 结论: 。 |
| 步骤二:将步骤一的浊液过滤,取滤液于试管中B中,加入 , 振荡,观察 | 现象: ; 结论:样品中含有NaHCO3。 |
| 步骤三:将步骤二的浊液过滤,取滤液于试管C中, 振荡,观察 | 现象: ; 结论: 。 |
| 步骤一:取少量制品于试管中,加入少量蒸馏水,振荡,溶解:往试管中加入 过量的Ba(NO3)2溶液,振荡,观察 (2分) | 现象:溶液中产生大量白色沉淀; 结论:试样中含有Na2CO3。(1分) |
| 步骤二:将步骤一的浊液过滤:取滤液于试管B中,加入 适量的NaOH溶液, 振荡,观察(1分) | 现象:有少量白色沉淀生成 ;(1分) 结论:试样中含有NaHCO3。 |
| 步骤三: 将步骤二的浊液过滤后,取滤液于试管C中,先加入足量的稀硝酸,再加入少许AgNO3溶液,振荡,观察(2分) | 现象:有少量白色沉淀生成 ; 结论:试样中含有NaCl 。(1分) |


 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
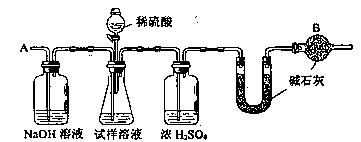
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
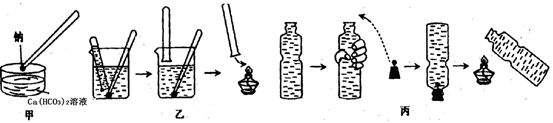
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | | 氨碱法 | 联合制碱法 |
| A | 原料 | 食盐、氨气、生石灰 | 食盐、氨气、二氧化碳 |
| B | 可能的副产物 | 氯化钙 | 氯化铵 |
| C | 循环物质 | 氨气、二氧化碳 | 氯化钠 |
| D | 评价 | 原料易得;设备复杂;能耗高 | 原料利用率高;废弃物少 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.钠与水反应放出的热使钠熔成一个小球 |
| B.钠浮在水面上,四处游动 |
| C.钠消失后,向烧杯中滴入几滴酚酞试液,溶液仍为无色 |
| D.钠消失后,在烧杯中投入少量铝,有气体产生 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com