
����ͭ��һ������Ũ���ᷴӦ���õ�����ͭ��Һ��NO2��NO�Ļ������2.24L����״��������Щ������һ�����O2����״������Ϻ�ͨ��ˮ�У�����������ȫ��ˮ�����������ᡣ������������ͭ��Һ�м���4mol•L��1NaOH��Һ��Cu2+ǡ����ȫ������������NaOH��Һ�������50mL������˵����ȷ���ǣ� ��
A���μӷ�Ӧ��������0.2mol B���������������Ϊ1.68 L
C��ͭ�����ᷴӦ������ת�Ƶĵ���Ϊ0.3 mol D����������к�NO21.12 L

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ�߶�10���¿���ѧ���������棩 ���ͣ�ѡ����
��4 mol A�����2 mol B������2 L�������л�ϣ�����һ�������·������·�Ӧ��2A��g����B��g�� 2C��g������2 s����C��Ũ��Ϊ0.6 mol��L��1���������м���˵����
2C��g������2 s����C��Ũ��Ϊ0.6 mol��L��1���������м���˵����
��������A��ʾ�ķ�Ӧ��ƽ������Ϊ0.3 mol��L��1��s��1
��������B��ʾ�ķ�Ӧ��ƽ������Ϊ0.6 mol��L��1��s��1
��2 sʱ����A��ת����Ϊ70%
��2 sʱ����B��Ũ��Ϊ0.7 mol��L��1��������ȷ����
A���٢� B���٢� C���ڢ� D���ۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ɹŸ߶������л�ѧ���������棩 ���ͣ�ѡ����
���������к�ƻ���ס�ƻ������һ����ƻ�����Ͷ��ɵ����нⶾ����֬�����ʺ�ֹк������ҩЧ�Ľ���ʳƷ��ƻ���ᣨ��?�ǻ������ᣩ���������ϵ���Ҫ�������ʣ�ƻ����Ľṹ������ʾ���������˵������ȷ���ǣ� ��
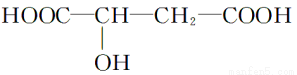
A��ƻ������һ���������ܷ���������Ӧ
B��ƻ������һ���������ܷ�����������Ӧ
C��ƻ������һ���������ܷ�����ȥ��Ӧ
D��1 molƻ������Na2CO3��Һ��Ӧ��������2 mol Na2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�߶������л�ѧ���������棩 ���ͣ�ѡ����
һ����̬������һ����̬ϩ���Ļ����9 g�����ܶ�����ͬ����������Ŀ�ĵ�11.25�������������ͨ����������ˮʱ����ˮ����4.2 g������������̬���ǣ� ��
A���������ϩ B������Ͷ�ϩ C������ͱ�ϩ D���������ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ��������У������ѧ�����л�ѧ�Ծ��������棩 ���ͣ������
�������ƣ�CaO2��8H2O����һ����ˮ����ֳ�й㷺ʹ�õĹ�������
��1��Ca��OH��2����Һ��H2O2��Һ��Ӧ���Ʊ�CaO2��8H2O��
Ca��OH��2+H2O2+6H2O CaO2��8H2O��Ӧʱͨ�����������Ca��OH��2����Ŀ���� ��
CaO2��8H2O��Ӧʱͨ�����������Ca��OH��2����Ŀ���� ��
��2�������ˮ�м���һ������CaO2��8H2O����ˮ��Ũ�����ӵ�������____________������ţ���
A��Ca2+ B��H+ C��CO32- D��OH?
��3��ˮ���ܽ����IJⶨ�������£���һ����ˮ���м�������MnSO4�ͼ���KI��Һ������MnO��OH��2 �������ܷ⾲�ã���������ϡH2SO4����MnO��OH��2��I?��ȫ��Ӧ����Mn2+��I2���Ե�����ָʾ������Na2S2O3����Һ�ζ����յ㣬�ⶨ���������ʵ�ת����ϵ���£�
�������ܷ⾲�ã���������ϡH2SO4����MnO��OH��2��I?��ȫ��Ӧ����Mn2+��I2���Ե�����ָʾ������Na2S2O3����Һ�ζ����յ㣬�ⶨ���������ʵ�ת����ϵ���£�
O2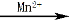 MnO��OH��2
MnO��OH��2 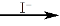 I2
I2  S4O62?
S4O62?
��д��O2��Mn2+������MnO��OH��2�����ӷ���ʽ ��
��ȡ�ӹ�һ����CaO2��8H2O�ij���ˮ��100.00 mL�������������ⶨˮ���ܽ�����������0.01000 mol��L?1 Na2S2O3����Һ13.50 mL�������ˮ���е��ܽ���Ϊ mg��L?1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ��������У������ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
25��Cʱ��ij��ѧʵ��С��ͬѧ���ô���ʯ��ϡ�����Ʊ�CO2��IJ���Һ�еμ�̼������Һ������Һ�в���pH�����������pH�仯������ͼ��ʾ������˵������ȷ���ǣ� ��
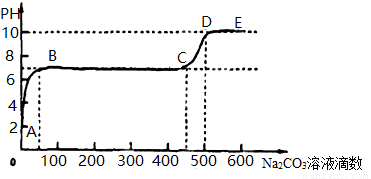
A����ʼʱ��ҺpH��2����Ϊ����Һ�л�������ʣ��
B��BC�α�ʾ����̼������Һ�ĵ��룬CaCO3����������������
C������500��̼������Һ����Һ��c��OH������c��H+��
D��AB�����ķ�ӦΪ��Ca2+ + CO32��== CaCO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ��������У������ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��������ˮ�м��������������ʣ�����ǿ��ҺƯ���������ǣ� ��
A��̼��Ʒ�ĩ B��ϡ���� C���Ȼ�����Һ D����������ˮ��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��㶫ʡ�����и�����ѧ�ڵ���һ��ѧ�Ծ��������棩 ���ͣ������
����ѧ-��ѧ�뼼����
��ҵ����������(��Ҫ�ɷ�ΪAl2O3��������Fe2O3��SiO2)Ϊԭ��ұ����������ͼ��ʾ��
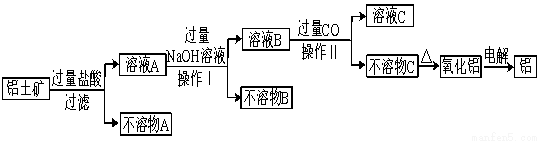
��1�� ʵ���ҽ��й����õ��IJ����������ձ���_____________��_____________��
��2�� ����II�����ɲ�����C�����ӷ���ʽ�� ��
��3�� ���������۵�ߴ�2050�棬��ҵ��Ϊ�����ܺģ������ĵ��ұ��ʱ����ȡ�Ĵ�ʩ�� ��
��4�� ���ұ����ʱ��������������̼�ز����Ƴɣ��������У����������趨�ڽ��и�����ԭ���� ��
��5�� Ϊ������ۺϾ���Ч�棬ʵ�ʹ�ҵ�����г���������Ӧ�е��������ѭ�����á��䲿��ת����ϵ����ͼ��ʾ��
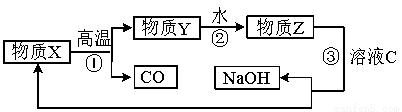
�� ����ת����δ�漰���ֻ�����Ӧ�����е� ��Ӧ��
�� д�����̢۵Ļ�ѧ����ʽ�� ��
��6�� �о��������������������Ԫ�ػ�����Σ�����彡����������ʵ����������ž���Ԫ�ع�������Ĵ�ʩ��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�������и��������л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ����٤��������ֵ������˵����ȷ����
A���������������з�Ӧ��1 mol��ʧȥ�ĵ�����Ϊ3 NA
B��6.4 g Cu���������ַ�Ӧ��ת�Ƶ�����Ϊ0.2 NA
C���ܱ�������2 mol NO��1 mol O2��ַ�Ӧ����ķ�����ΪNA
D�����³�ѹ�£�0.1 mol NH3��0.1 mol HCl��ַ�Ӧ�����ò��ﺬ0.1 NA������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com