
药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
下列有关叙述正确的是
A.贝诺酯分子中有三种含氧官能团
B.可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚
C.乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应
D.贝诺酯与足量NaOH溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
科目:高中化学 来源: 题型:
按要求完成下列问题。
(1)写出NH3的电子式: 。 (2) 写出基态Cr原子的简化电子排布式 :_______。
(3)写出基态 Mg2+的电子排布图: 。 (4) 写出Zn原子的价电子排布式 :____________。
(5)将Al、Si、P、S的第一电离能由小到大排列为 。
(6) 指出配合物K3[Co(CN)6]中的中心离子、配位体及其配位数:________、________、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
随着人们生活节奏的加快,方便的小包装食品已被广泛接受。为了延长食品的保质期,防止食品受潮及富脂食品氧化变质,在包装袋中应放入的化学物质是( )
A.无水硫酸铜、蔗糖 B.食盐、硫酸亚铁
C.生石灰、硫酸亚铁 D.生石灰、食盐
查看答案和解析>>
科目:高中化学 来源: 题型:
等物质的量的N2、O2、CO2混合气体通过Na2O2后,体积变为原体积的8/9 (同温同压),这时混合气体中N2、O2、CO2物质的量之比为( )
A.3∶4∶1 B.3∶3∶2 C.6∶7∶3 D.6∶9∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与科学、技术、社会、环境密切相关。下列有关说法中错误的是
A.节日燃放的焰火是某些金属元素焰色反应所呈现出来的色彩
B.小苏打是制作馒头和面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂
C.为防止中秋月饼等富脂食品因被氧化而变质,常在包装袋中放入生石灰或硅胶
D.面粉中禁止添加CaO2 、过氧化苯甲酰等增白剂,CaO2属于过氧化物,过氧化苯甲酰属于有机物
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸是工业生产中最为重要的产品之一,在化学工业的很多领域都要用到浓硫酸。
 (1)在硫酸工业生产中,我国采用黄铁矿为原料生产SO2,反应的化学方程式为: ,该反应在 中进行(填仪器名称)。
(1)在硫酸工业生产中,我国采用黄铁矿为原料生产SO2,反应的化学方程式为: ,该反应在 中进行(填仪器名称)。
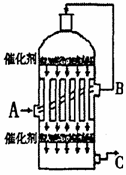
(2)为了有利于SO2转化为SO3,且能充分利用热能,采用了多层催化剂
且有热交换器的 (填仪器名称)中进行反应。在如图所示的装置中, C处流出的气体有 ;SO3进入 (填仪器名称)用 吸收,得到浓硫酸或发烟硫酸。
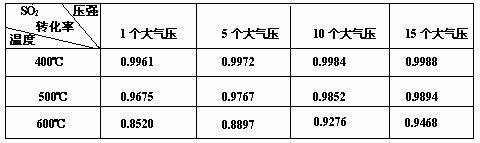
(3)实验测得SO2反应生成SO3的转化率与温度、压强有关,请根据下
表信息,结合工业生产实际,选择最合适的生产条件是 。
 |
(4)现在欲提高SO2的反应速率和转化率,下列措施可行的是 。
A、向装置中通入氮气且保持体积不变 B、向装置中通入氧气且保持体积不变
C、添加更多的催化剂 D、降低温度,及时转移SO3
(5)由吸收塔排出的尾气中有SO2的含量如果超过500μL/ L,就要加以处理后才能排出,处理方法之一是用氨水洗涤烟气脱硫,用方程式表示氨水洗涤吸收塔排除的尾气的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知胆矾溶于水时溶液温度降低,胆矾分解的热化学方程式为:
CuSO4•5H2O(s)=CuSO4(s)+5H2O(l) △H= +Q1 kJ/mol
室温下,若将1 mol无水硫酸铜溶解为溶液时放热Q2kJ,则( )
A.Q1>Q2 B.Q1=Q2 C.Q1<Q2 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
如下图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极。将直流电源接通后,F极附近呈红色。请回答:
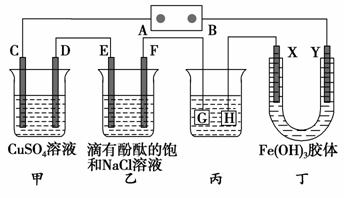
(1)B极是电源的________,一段时间后,甲中溶液颜色________,丁中X极附近的颜色逐渐变浅,Y极附近的颜色逐渐变深,这表明____________________,在电场作用下向Y极移动。
(2)若甲、乙装置中的C、D、E、F电极均只有一种单质生成时,对应单质的物质的量之比为______________。
(3)现用丙装置给铜件镀银,则H应该是________(填“镀层金属”或“镀件”),电镀液是________溶液。当乙中溶液的pH是13时(此时乙溶液体积为500 mL),丙中镀件上析出银的质量为________,甲中溶液的pH________(填“变大”、“变小”或“不变”)。
(4)若将C电极换为铁,其他装置都不变,则甲中发生总反应的离子方程式是_______________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化铜有多种用途,如作玻璃着色剂、油类脱硫剂等。为获得纯净的氧化铜以探究其性质,某同学用工业硫酸铜(含硫酸亚铁等杂质)进行如 下实验:
下实验:
⑴制备氧化铜
工业CuSO4
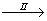 CuSO4溶液
CuSO4溶液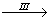 CuSO4·5H2O
CuSO4·5H2O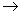 ……
……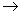 CuO
CuO
①步骤Ⅰ的目的是除不溶性杂质,操作是:___________________________。
②步骤Ⅱ的目的是除铁,操作是:滴加H2O2溶液,稍加热;当Fe2+完全转化后, 慢慢加入Cu2(OH)2CO3粉末,搅拌,以控制pH =3.5;加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH =1。控制溶液pH =3.5的原因是: 。
慢慢加入Cu2(OH)2CO3粉末,搅拌,以控制pH =3.5;加热煮沸一段时间,过滤,用稀硫酸酸化滤液至pH =1。控制溶液pH =3.5的原因是: 。
③步骤Ⅲ的目的是得到CuSO4·5H2O固体,操作是: 、过滤、水浴加热烘干。水浴加热的特点是:_________________________________。
⑵探究氧化铜的性质
①取A、B两支试管,往A中加入适量的CuO粉末,再分别向A和B加入等体积3% H2O2溶液,只观察到A中有大量气泡,结论是:______________________。
②为探究试管A中的反应速率,收集气体并测定其体积必需的实验仪器有: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com