
【题目】七铝十二钙(12CaO·7Al2O3)是新型的超导材料和发光材料,用白云石(主要含CaCO3和MgCO3)和废Al片制备七铝十二钙的工艺如下:
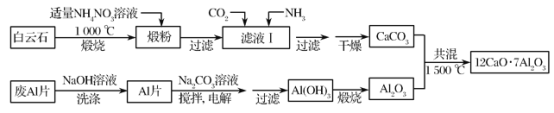
(1)煅粉主要含MgO和________,用适量NH4NO3溶液浸取煅粉后,镁化合物几乎不溶,若溶液Ⅰ中c(Mg2+)小于5×10-6mol·L-1,则滤液pH大于________[Mg(OH)2的Ksp=5×10-12];该工艺中不能用(NH4)2SO4代替NH4NO3,原因是______________。
(2)滤液Ⅰ中的阴离子有________(忽略杂质成分的影响);若滤液Ⅰ中仅通入CO2,会生成________,从而导致CaCO3产率降低。
(3)用NaOH溶液可除去废Al片表面的氧化膜,反应的离子方程式为_________。
(4)电解制备Al(OH)3时,电极分别为Al片和石墨,电解总反应方程式________。
(5)一种可超快充电的新型铝电池,充放电时AlCl4-和Al2Cl7-两种离子在Al电极上相互转化,其他离子不参与电极反应,放电时负极Al的电极反应式为_________。
【答案】CaO 11 加入(NH4)2SO4会生成CaSO4微溶物,在过滤时会被除去,造成生成的CaCO3减少 NO3-和OH- Ca(HCO3)2 2OH-+Al2O3=2AlO2-+H2O 2Al+6H2O![]() 2Al(OH)3↓+3H2↑ Al-3e-+7AlCl4-=4Al2Cl7-
2Al(OH)3↓+3H2↑ Al-3e-+7AlCl4-=4Al2Cl7-
【解析】
(1)白云石高温煅烧,CaCO3和MgCO3受热分解生成CaO和MgO,煅粉主要含有CaO和MgO。若溶液Ⅰ中c(Mg2+)小于5×10-6mol·L-1,根据Ksp=c(Mg2+)·c2(OH-)得:c(OH-)>![]() mol·L-1=1×10-3 mol·L-1,c(H+)<1×10-11mol·L-1,即pH>11。若用(NH4)2SO4代替NH4NO3,则(NH4)2SO4会与CaO反应生成CaSO4微溶物,在过滤时会被除去,造成生成的CaCO3减少。
mol·L-1=1×10-3 mol·L-1,c(H+)<1×10-11mol·L-1,即pH>11。若用(NH4)2SO4代替NH4NO3,则(NH4)2SO4会与CaO反应生成CaSO4微溶物,在过滤时会被除去,造成生成的CaCO3减少。
(2)煅粉的主要成分是CaO和MgO,加入适量NH4NO3溶液浸取煅粉后,由于镁化合物几乎不溶,则溶液中溶质主要为生成的Ca(NO3)2和Ca(OH)2,故滤液Ⅰ中的主要阴离子为NO3-和OH-。由于滤液Ⅰ的pH大于11,溶液中含有Ca(NO3)2和少量的NH4NO3与Ca(OH)2,若仅通入CO2会生成Ca(HCO3)2,从而导致CaCO3产率降低。
(3)用NaOH溶液可除去废Al片表面的氧化膜,反应的离子方程式为2OH-+Al2O3=2AlO2-+H2O。
(4)电解制备Al(OH)3时,电极分别为Al片和石墨,电解总反应方程式2Al+6H2O![]() 2Al(OH)3↓+3H2↑。
2Al(OH)3↓+3H2↑。
(5)由题意可知,放电时负极Al失去电子与AlCl4-结合生成Al2Cl7-,其电极反应式为Al-3e-+7AlCl4-=4Al2Cl7-。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 氢氧燃料电池放电时化学能全部转化为电能
B. 反应4Fe(s)+3O2(g)![]() 2Fe2O3(s)常温下可自发进行,该反应为吸热反应
2Fe2O3(s)常温下可自发进行,该反应为吸热反应
C. 3 mol H2与1 mol N2混合反应生成NH3,转移电子的数目小于6×6.02×1023
D. 在酶催化淀粉水解反应中,温度越高淀粉水解速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图是碳和水蒸气发生反应生成CO、H2的途径和三个状态的能量,该反应为吸热反应,比较E1、E2、E3的大小:_____。

(2)已知2mol氢气燃烧生成液态水时放出572kJ的热量,反应方程式是2H2(g)+O2(g)═2H2O(l)。请回答下列问题:
①该反应的生成物能量总和____(填“大于”、“小于”或“等于”)反应物能量总和。
②若2mol氢气完全燃烧生成水蒸气,则放出的热量____(填“大于”、“小于”或“等于”)572kJ。
(3)已知拆开1molN﹣N键、1molN﹣H键、1molN≡N键、O=O键需要的能量分别是3akJ、2.5akJ、8akJ、4akJ,完全燃烧1mol火箭燃料肼(N2H4)生成氮气和水蒸气放出能量为5akJ,则1molH2O(g)完全断键时共吸收____kJ的能量。
(4)已知化学反应A2(g)+B2(g)═2AB(g)的能量变化如图所示,反应物的总键能_____(填“大于”、“小于”或“等于”)生成物的总键能。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铝粉与某铁的氧化物FeO·2Fe2O3粉末配制成铝热剂,分成两等份。一份直接放入足量的烧碱溶液中,充分反应后放出气体在标准状况下的体积为3.92 L;另一份在高温下恰好反应完全,反应后的混合物与足量的盐酸反应后,放出的气体在标准状况下的体积为
A. 2.80 LB. 3.92 LC. 5.60 LD. 7.84 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光谱研究表明,易溶于水的SO2所形成的溶液中存在着下列平衡:

据此,下列判断中正确的是( )
A.该溶液中存在着SO2分子
B.该溶液中H+浓度是SO32-浓度的2倍
C.向该溶液中加入足量的酸都能放出SO2气体
D.向该溶液中加入过量NaOH可得到Na2SO3、NaHSO3和NaOH的混合溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五种短周期元素X、Y、Z、M、N,其原子半径与原子序数的关系如图,下列说法错误的是( )

A. 非金属性:X>Z
B. 气态氢化物的稳定性:M<N
C. X和Y形成的化合物只可能含离子键
D. M最高价氧化物对应的水化物是一种弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实中不能用平衡移动原理解释是( )
A. 密闭、低温是存放氨水的必要条件
B. 实验室常用排饱和食盐水法收集氯气
C. 打开汽水瓶时,有大量气泡冒出
D. 已知合成氨的反应为N2(g)+3H2(g)2NH3(g)△H=﹣92.4 kJ/mol,工业上采用较高温度和使用催化剂以提高氨气的产率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中A~H均为中学化学中常见的物质,A、B、H为气体,反应①是重要的工业反应,它们之间有如下转化关系(反应中生成的水已略去)。

请回答以下问题:
(1)B是________,D是________,G是________,H是________(填化学式)。
(2)工业上常利用反应①制取漂白粉,该反应的化学方程式:_____________________,漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为__________________________。
(3)A中元素的原子结构示意图为________________。
(4)上述反应中属于氧化还原反应的是_________(填写序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)当前,环境治理已成为重要的民生工程。
①2014年1月,教育部规定在学校公共场所禁止吸烟。下列有关说法中不正确的是_____(填字母代号,下同)。
A.吸烟会对室内和公共场所造成污染
B.吸入焦油、尼古丁及颗粒物可导致多种病变
C.N2、 CO2、CO和尼古丁都属于室内空气污染物
②下列做法可能会加重“雾霾”的是______。
A.大量焚烧秸杆
B.在汽车尾气系统装置催化转化器
C.发展煤的气化和液化等洁净煤技术
③下列处理垃圾的方法中,不正确的是____。
A.回收利用废纸
B.回收利用易拉罐
C.填埋废旧电池
④垃圾处理遵循无害化、减量化和资源化的原则。垃圾分类收集是实观上述原则的措施之—。贴有下图标示,表示为________
![]()
A.可回收物 B.有害垃圾 C.其他垃圾
⑤我国城市发布的“空气质量日报”中,下列物质不列入首要污染物的是____。
A.二氧化硫 B.二氧化碳 C.二氧化氮 D.可吸入颗粒物
(2)材料是人类赖以生存和发展的重要物质基础。
①试管、烧怀和烧瓶等化学仪器的主要材质是____ (填字母代号)。
A.玻璃 B. 陶瓷
②钢铁是目前用最大的铁合金。钢铁接触海水发生电化学腐蚀,其负极反应式为______;因此,为防止轮船船体被腐蚀,可在船体上安装一定量的______(填“锌”成“铜”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com