
| A、气态氢化物的热稳定性:A<C |
| B、元素A与B只能形成一种化合物 |
| C、元素B与D形成的化合物是离子化合物 |
| D、最高价氧化物对应的水化物的酸性:C>D |


科目:高中化学 来源: 题型:
| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
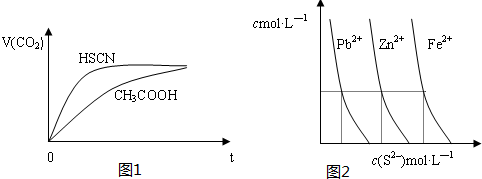
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、碳酸氢钙溶液和氢氧化钠溶液混合:HCO3-+OH-═CO32-+H2O |
| B、碳酸钙与醋酸反应:CaCO3+2H+═Ca2++H2O+CO2↑ |
| C、硝酸铝溶液中加入过量氨水:Al3++NH3?H2O═AlO2-+4NH4++2H2O |
| D、硫酸铜溶液和氢氧化钡溶液混合:Cu2++SO42-+Ba2++2OH-═BaSO4↓+Cu(OH)2↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、汽车尾气的大量排放影响了空气的质量,但是不会造成PM2.5值升高 |
| B、研发安全特效药物,有利于抵御人类疾病 |
| C、规范食品添加剂的生产和科学使用,有利于保障人体健康和生命安全 |
| D、推广城市生活垃圾处理的减量化、资源化和无害化技术,有利于环境保护和资源充分利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 在一个固定容积的密闭容器中发生如下反应:
在一个固定容积的密闭容器中发生如下反应:| △ |
| A、处于平衡状态的只有t1~t2段 |
| B、t1~t2段c(NH3)最大 |
| C、在t2时可能是向容器中充入了少量He |
| D、在t4时可能是升高温度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2O2是氧化剂,H2O2中的氧元素被还原 |
| B、每生成1mol O2转移的电子的物质的量为4mol |
| C、ClO2中的氯元素被氧化 |
| D、ClO2是氧化剂,H2O2是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCOOH+H2O?HCOO-+H3O+ |
| B、H2O+HCO3-?OH-+H2CO3 |
| C、CO32-+H2O?HCO3-+OH- |
| D、HS-+H2O?H2S+OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙酸与碳酸钠溶液反应:2H++CO32-═CO2↑+H2O | ||||
| B、醋酸溶液与新制氢氧化铜反应:CH3COOH+OH-→CH3COO-+H2O | ||||
C、苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O
| ||||
D、乙醛溶液与足量的银氨溶液共热 CH3CHO+2[Ag(NH3)2]++2OH-
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com