
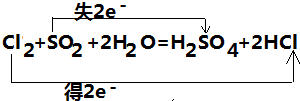
分析 该反应中,Cl元素化合价由0价变为-1价、S元素化合价由+4价变为+6价,得电子的反应物是氧化剂、失电子的反应物是还原剂,氧化剂被还原、还原剂被氧化,还原剂对应的产物是氧化产物,结合化合价的变化计算电子转移.
解答 解:(1)该反应中,Cl元素化合价由0价变为-1价、S元素化合价由+4价变为+6价,其转移电子数是2,转移电子数目和方向为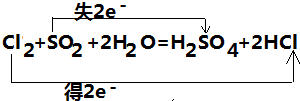 ,
,
故答案为: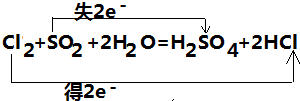
(2)该反应中,Cl元素化合价由0价变为-1价、S元素化合价由+4价变为+6价,所以Cl2是氧化剂、SO2是还原剂,则被氧化的元素是S元素,还原剂对应的产物H2SO4是氧化产物;
故答案为:Cl2;S;H2SO4;
(3)该反应中,Cl元素化合价由0价变为-1价、S元素化合价由+4价变为+6价,其转移电子数是2,当有2mol的水完全参与反应时,有2mol电子转移;
故答案为:2.
点评 本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,题目难度不大.


 快捷英语周周练系列答案
快捷英语周周练系列答案科目:高中化学 来源: 题型:选择题
| A. | NH4Br的电子式  | |
| B. | S2-的结构示意图 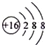 | |
| C. | 乙烯的分子式 CH2=CH2 | |
| D. | 原子核内有l7个中子的氯原子${\;}_{17}^{35}$Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验方案 |
| A | 检验食盐中是否添加KIO3 | 取食盐试样,溶于KI溶液,加入淀粉溶液,观察溶液是否变蓝 |
| B | 验证硝酸是挥发性酸 | 用两根玻璃棒分别蘸取浓硝酸和浓氨水,然后靠近,观察是否有白烟产生 |
| C | 验证Br2氧化性强于Fe3+ | 取少许FeCl3晶体溶于稀盐酸,加入KSCN观察溶液是否变红,滴入溴水后再观察是否变红 |
| D | 验证氯酸钾中含有氯元素 | 取少量氯酸钾加入MnO2充分加热,残留物溶于水,取上层清液,滴入硝酸酸化的AgNO3溶液,观察是否有白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 除杂试剂 | 方法 | |
| C6H6 (C6H5OH) | ||
| C2H6 (C2H4) | ||
| C6H5Br (Br2) | . |
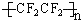 ,类型加聚反应.
,类型加聚反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H2 | B. | C2H5OH | C. | CH3CHO | D. | CH3COOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶质的质量分数为w=$\frac{a}{Vρ-a}$×100% | |
| B. | 上述溶液中再加入V mL水后,所得溶液溶质的质量分数大于0.5w | |
| C. | 上述溶液中再加入相同质量的水后,所得溶液的物质的量浓度变为原来一半 | |
| D. | 溶质的物质的量浓度c=$\frac{1000a}{17V}$ mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何可逆反应都有一定的限度,且限度是可以改变的 | |
| B. | 对任何化学反应来说,反应速率越大,则现象越明显 | |
| C. | 决定化学反应速率的主要因素是温度、浓度、压强 | |
| D. | 铁与稀硫酸反应制氢气时,改用98.3%的浓硫酸,对增大化学反应速率明显有效 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯化铜溶液中加入氢氧化铁 | B. | 硝酸铝溶液中加入氢氧化钠 | ||
| C. | 氢氧化钾溶液中加入硫化铜 | D. | 碳酸钠中加入氢氧化钾 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com