
离子化合物X完全是由短周期元素组成的,其中一个阳离子和一个阴离子核外电子数之和为20。则下列有关X的说法中正确的是( )
A.X中阳离子和阴离子个数不一定相等
B.X中一定有离子键,一定不含共价键
C.若X只含两种元素,则这两种元素可在同一周期也可在同一主族
D.X中阳离子半径一定大于阴离子半径
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
油脂皂化后,要使肥皂和甘油从混合物里充分分离,可采用①分液 ②蒸馏 ③过滤 ④盐析 ⑤渗析中的_________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知正己烷的球棍模型为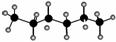 。某有机物a的分子式和正己烷相同,且主链上有4个碳原子,则下列关于a的观点正确的是 ( )。
。某有机物a的分子式和正己烷相同,且主链上有4个碳原子,则下列关于a的观点正确的是 ( )。
A.a分子中可能有三个甲基
B.a的分子式为C6H10
C.a的一氯代物可能有三种
D.在光照条件下,a能与溴的四氯化碳溶液发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”。
(1)离子晶体除含离子键外,一定不含其他化学键(×)
(2)离子晶体中一定含有金属阳离子(×)
(3)离子晶体的熔点一定低于原子晶体(×)
(4)含有阳离子的晶体一定是离子晶体(×)
(5)离子晶体中一定不含分子(×)
(6)金属与非金属形成的化合物一定都是离子化合物(×)
(7)具有金属光泽且能导电的单质一定是金属(×)
(8)金属晶体的熔点差别很大,有的很高(如钨),有的很低(如汞)(√)
查看答案和解析>>
科目:高中化学 来源: 题型:
4种相邻主族短周期元素的相对位置如表,元素x的原子核外电子数是m的2倍,y的氧化物具有两性。回答下列问题:
| m | n | ||
| x | y |
(1)元素x在周期表中的位置是______周期第______族,其单质可采用电解熔融__________的方法制备。
(2)m、n、y三种元素最高价氧化物的水化物中,酸性最强的是__________,碱性最强的是______________。(填化学式)
(3)气体分子(mn)2的电子式为__________。(mn)2称为拟卤素,性质与卤素类似,其与氢氧化钠溶液反应的化学方程式为________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对三硫化四磷分子的结构研究表明,该分子中没有不饱和键,且各原子的最外层均已达到了8个电子的稳定结构。则一个三硫化四磷分子中含有的共价键个数是( )
A.7个 B.9个 C.19个 D.不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
依据下列甲、乙、丙三图,判断下列叙述不正确的是( )
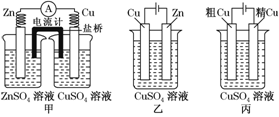
A.甲是原电池,乙是电镀装置
B.甲、乙装置中,锌极上均发生氧化反应
C.乙、丙装置中,阳极均发生氧化反应而溶解
D.乙、丙装置中,c(Cu2+)基本不变
查看答案和解析>>
科目:高中化学 来源: 题型:
在等温等容条件下,可逆反应:2A(g)+B(g)3C(g)+D(s)起始物质的量如下表所示:
| 序号 | A | B | C | D |
| ① | 2 mol | 1 mol | 0 | 0 |
| ② | 4 mol | 2 mol | 0 | 0 |
| ③ | 1 mol | 0.5 mol | 1.5 mol | 0.5 mol |
| ④ | 0 | 1 mol | 3 mol | 1 mol |
| ⑤ | 0 | 0 | 3 mol | 1 mol |
上述反应达到平衡时,互为等效平衡的是哪几组?达到平衡后,哪些量相同?
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关金属的说法中,不正确的是( )
A.青铜、不锈钢、硬铝都是合金
B.铜表面易形成致密的氧化膜
C.工业上用电解熔融MgCl2的方法制取金属镁
D.铝是活泼金属,但在空气中耐腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com