
°±»ł¼×Ėįļ§£ØNH2COONH4£©ŹĒŅ»ÖÖ°×É«¹ĢĢ壬Ņ×·Ö½ā”¢Ņ×Ė®½ā£¬æÉÓĆ×ö·ŹĮĻ”¢Ćš»š¼Į”¢Ļ“µÓ¼ĮµČ”£Ä³»ÆѧŠĖȤŠ”×éÄ£Äā¹¤ŅµŌĄķÖʱø°±»ł¼×Ėįļ§£¬
·“Ó¦µÄ»Æѧ·½³ĢŹ½ČēĻĀ£ŗ
2NH3(g)+CO2(g)  NH2COONH4(s) ¦¤H£¼0
NH2COONH4(s) ¦¤H£¼0
£Ø1£©ČēÓĆÓŅĶ¼×°ÖĆÖĘČ”°±Ęų£¬ÄćĖłŃ”ŌńµÄŹŌ¼ĮŹĒ ”£

£Ø2£©Öʱø°±»ł¼×Ėįļ§µÄ×°ÖĆČēĻĀĶ¼ĖłŹ¾£¬°Ń°±ĘųŗĶ¶žŃõ»ÆĢ¼ĶØČėĖÄĀČ»ÆĢ¼ÖŠ£¬²»¶Ļ½Į°č»ģŗĻ£¬Éś³ÉµÄ°±»ł¼×Ėįļ§Š”¾§ĢåŠüø”ŌŚĖÄĀČ»ÆĢ¼ÖŠ”£µ±Šüø”Īļ½Ļ¶ąŹ±£¬Ķ£Ö¹Öʱø”£
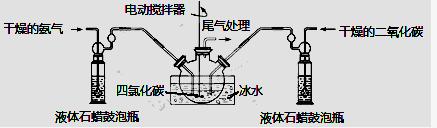
×¢£ŗĖÄĀČ»ÆĢ¼ÓėŅŗĢåŹÆĄÆ¾łĪŖ¶čŠŌ½éÖŹ”£
¢Ł·¢ÉśĘ÷ÓƱłĖ®ĄäČ“µÄŌŅņŹĒ£ŗ ”¢ ”£ŅŗĢåŹÆĄÆ¹ÄÅŻĘæµÄ×÷ÓĆŹĒ£ŗ ”£
¢Ś“Ó·“Ó¦ŗóµÄ»ģŗĻĪļÖŠ·ÖĄė³ö²śĘ·£¬ĪŖĮĖµĆµ½øÉŌļ²śĘ·£¬Ó¦²ÉČ”µÄ·½·ØŹĒ_______ £ØĢīŠ“Ń”ĻīŠņŗÅ£©”£
a.³£Ń¹¼ÓČČŗęøÉ b.øßŃ¹¼ÓČČŗęøÉ c.ÕęæÕ40 ”ęŅŌĻĀŗęøÉ
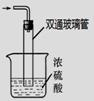
¢ŪĪ²Ęų“¦Ąķ×°ÖĆČēÓŅĶ¼ĖłŹ¾”£Ė«Ķز£Į§¹ÜµÄ×÷ÓĆ£ŗ £»
ÅØĮņĖįµÄ×÷ÓĆ£ŗ ”¢ ”£
£Ø3£©Č”Ņņ²æ·Ö±äÖŹ¶ų»ģÓŠĢ¼ĖįĒāļ§µÄ°±»ł¼×Ėįļ§ŃłĘ·11.73 g£¬ÓĆ×ćĮæŹÆ»ŅĖ® ³ä·Ö“¦Ąķŗó£¬Ź¹Ģ¼ŌŖĖŲĶźČ«×Ŗ»ÆĪŖĢ¼ĖįøĘ£¬¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ£¬²āµĆÖŹĮæĪŖ15.00 g”£Ōņѳʷ֊°±»ł¼×Ėįļ§µÄĪļÖŹµÄĮæ·ÖŹżĪŖ ”£
[Mr(NH2COONH4)=78g/mol”¢Mr(NH4HCO3) =79 g/mol”¢Mr(CaCO3)=100 g/mol]”¾Ą“.Ō“£ŗČ«,
”¾ÖŖŹ¶µć”æ³£¼ūŹµŃé²Ł×÷²½Öč”¢ŹµŃé·½°øµÄÉč¼ĘÓėĘĄ¼Ū
”¾“š°ø½āĪö”æ £Ø1£©ÅØ°±Ė®ÓėĒāŃõ»ÆÄĘ¹ĢĢå £ØCaO”¢¼īŹÆ»Ņ£©µČŗĻĄķ“š°ø£Ø2·Ö£©
£Ø2£©¢Ł½µĪĀĢįøß·“Ó¦ĪļÖŹ×Ŗ»ÆĀŹ£Ø»ņ½µµĶĪĀ¶Č£¬·ĄÖ¹Ņņ·“Ó¦·ÅČČŌģ³É²śĪļ·Ö½ā£©£Ø2·Ö£©
Ķعż¹Ū²ģĘųÅŻ£¬µ÷½ŚNH3ÓėCO2ĶØČė±ČĄż£Ø2·Ö£©
¢Ś¹żĀĖ£Ø2·Ö£© C £Ø2·Ö£©
¢Ū·ĄÖ¹µ¹Īü£Ø1·Ö£©ĪüŹÕ¶ąÓą°±Ęų·ĄÖ¹æÕĘųÖŠĖ®ÕōĘų½ųČė·“Ó¦Ę÷Ź¹°±»ł¼×Ėįļ§Ė®½ā£Ø2·Ö£©
£Ø3£©80% £Ø 4/5”¢0.8ĘäĖū½į¹ū²»øų·Ö£©£Ø2·Ö£©
½āĪö£ŗ£Ø1£©×°ÖĆ1ŹĒĄūÓĆ·ÖŅŗĀ©¶·µĪČėŅŗĢåČܽā׶ŠĪĘæÖŠµÄ¹ĢĢ壬ĄūÓĆČܽā·ÅČČŹ¹°±Ė®·Ö½āÉś³É°±Ęų£»°ŃÅØ°±Ė®µĪ¼Óµ½¹ĢĢåŃõ»ÆøĘ»ņĒāŃõ»ÆÄĘ£¬ŌŚČܽā¹ż³ĢÖŠ·ÅČČŹ¹ÅØ°±Ė®·Ö½āÉś³É°±Ęų£»£Ø2£©¢Ł·“Ó¦2NH3£Øg£©+CO2£Øg£©⇌NH2COONH4£Øs£©+Q£¬ŹĒ·ÅČČ·“Ó¦£¬½µĪĀĘ½ŗāÕżĻņ½ųŠŠ£¬ĪĀ¶ČÉżøߣ»·¢ÉśĘ÷ÓƱłĖ®ĄäČ“Ģįøß·“Ó¦ĪļÖŹ×Ŗ»ÆĀŹ£¬·ĄÖ¹Éś³ÉĪļĪĀ¶Č¹żøß·Ö½ā£¬ŅŗĢåŹÆĄÆ¹ÄÅŻĘæµÄ×÷ÓĆŹĒæŲÖĘ·“Ó¦½ųŠŠ³Ģ¶Č£¬æŲÖĘĘųĢåĮ÷ĖŁŗĶŌĮĻĘųĢåµÄÅä±Č£»¢ŚÖʱø°±»ł¼×Ėįļ§µÄ×°ÖĆČēĶ¼ĖłŹ¾£¬°Ń°±ĘųŗĶ¶žŃõ»ÆĢ¼ĶØČėĖÄĀČ»ÆĢ¼ÖŠ£¬²»¶Ļ½Į°č»ģŗĻ£¬Éś³ÉµÄ°±»ł¼×Ėįļ§Š”¾§ĢåŠüø”ŌŚĖÄĀČ»ÆĢ¼ÖŠ£¬·ÖĄė²śĘ·µÄŹµŃé·½·ØĄūÓĆ¹żĀĖµĆµ½£¬°±»ł¼×Ėįļ§£ØNH2COONH4£©ŹĒŅ»ÖÖ°×É«¹ĢĢ壬Ņ×·Ö½ā”¢²»ÄܼÓČČŗęøÉ£¬Ó¦ŌŚÕęæÕ40”ęŅŌĻĀŗęøÉ£»¢ŪĖ«Ķز£Į§¹ÜµÄ×÷ÓĆŹĒ·ĄÖ¹ŅŗĢåµ¹Īü£»ÅØĮņĖįĘšµ½ĪüŹÕ¶ąÓąµÄ°±Ęų£¬Ķ¬Ź±·ĄÖ¹æÕĘųÖŠĖ®ÕōĘų½ųČė·“Ó¦Ę÷Ź¹°±»ł¼×Ėįļ§Ė®½ā£»£Ø3£©Č”Ņņ²æ·Ö±äÖŹ¶ų»ģÓŠĢ¼ĖįĒāļ§µÄ°±»ł¼×Ėįļ§ŃłĘ·11.73g£¬ÓĆ×ćĮæŹÆ»ŅĖ®³ä·Ö“¦Ąķŗó£¬Ź¹Ģ¼ŌŖĖŲĶźČ«×Ŗ»ÆĪŖĢ¼ĖįøĘ£¬¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ£¬²āµĆÖŹĮæĪŖ15.00g£®ĪļÖŹµÄĮæĪŖ0.15mol£¬Éčѳʷ֊°±»ł¼×Ėįļ§ĪļÖŹµÄĮæĪŖx£¬Ģ¼ĖįĒāļ§ĪļÖŹµÄĮæĪŖy£¬ŅĄ¾ŻĢ¼ŌŖĖŲŹŲŗćµĆµ½£»
x+y=0.15 ½āµĆx=0.12mol
78x+79y=11.73 y=0.03mol
Ōņѳʷ֊°±»ł¼×Ėįļ§µÄĪļÖŹµÄĮæ·ÖŹż=0.12mol”Ā0.15mol”Į100%=80%£»
”¾Ė¼Ā·µć²¦”æ±¾Ģāæ¼²éĮĖĪļÖŹÖʱøŹµŃéµÄÉč¼ĘÓ¦ÓĆ£¬Ö÷ŅŖŹĒ°±ĘųµÄÖʱø·½·Ø£¬°±»ł¼×ĖįµÄÖʱøŹµŃé×°ÖĆ·ÖĪöÅŠ¶Ļ£¬ŹµŃ黳±¾²Ł×÷£¬»ģŗĻĪļ·ÖĄėµÄŹµŃéÉč¼Ę£¬ÓŠ¹Ų»ģŗĻĪļµÄ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ”£


 ÓÅÉśĄÖŌ°ĻµĮŠ“š°ø
ÓÅÉśĄÖŌ°ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ÓĆFeCl3ČÜŅŗøÆŹ“Ó”Ė¢µēĀ·°åÉĻµÄĶ£¬ĖłµĆČÜŅŗÖŠ¼ÓČėĢś·Ū”£¶Ō¼ÓČėĢś·Ū³ä·Ö·“Ó¦ŗóµÄČÜŅŗ·ÖĪöŗĻĄķµÄŹĒ( )
A£®ČōĪŽ¹ĢĢåŹ£Óą£¬ŌņČÜŅŗÖŠŅ»¶ØÓŠFe3£«”” B£®ČōÓŠ¹ĢĢå“ęŌŚ£¬ŌņČÜŅŗÖŠŅ»¶ØÓŠFe2£«
C£®ČōČÜŅŗÖŠÓŠCu2£«£¬ŌņŅ»¶Øƻӊ¹ĢĢåĪö³ö”” D£®ČōČÜŅŗÖŠÓŠFe2£«£¬ŌņŅ»¶ØÓŠCuĪö³ö
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠ¹ŲÓŚµē»ÆѧÖŖŹ¶Ėµ·ØÕżČ·µÄŹĒ
A£®µē½āAlCl3ČÜŅŗ£¬ŌŚŅõ¼«ÉĻĪö³ö½šŹōAl
B£®ĒāŃõČ¼ĮĻµē³ŲÖŠ£¬ŃõĘųŹĒÕż¼«·“Ó¦Īļ
C£®ÓƶčŠŌµē¼«µē½āCuSO4ČÜŅŗŅ»¶ĪŹ±¼ä£¬ČÜŅŗĖįŠŌ²»±ä
D£®Ē¦Šīµē³ŲŌŚ³äµēŹ±£¬Į¬½ÓµēŌ“Õż¼«µÄµē¼«·“Ó¦ĪŖ£ŗPbSO4£«2e£=== Pb£«SO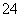
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĄūÓĆĻĀĮŠŹµŃé·½°øæÉŅŌ“Óŗ£Ńó¶ÆĪļ±śŗ£ĒŹÖŠĢįČ”¾ßÓŠæ¹Ö×Įö×÷ÓƵĻīŠŌĪļÖŹ”£ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ( )
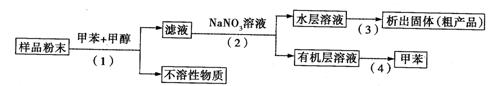
A£®²½Öč£Ø1£©ŠčŅŖ¹żĀĖ×°ÖĆ B£®²½Öč£Ø3£©ŠčŅŖÓƵ½Õō·¢Ćó
C£®²½Öč£Ø4£©ŹĒĄūÓĆĪļÖŹµÄ·Šµć²īŅģ½ųŠŠ·ÖĄėµÄ
D£®»īŠŌĪļÖŹŅ×ČÜÓŚÓŠ»śČܼĮ£¬ÄŃČÜÓŚĖ®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ä³Ń§ÉśÓĆĮæĶ²ĮæČ”ŅŗĢ壬³õ
“ĪŹÓĻßÓėĮæĶ²ÄŚ°¼ŅŗĆęµÄ×īµĶ“¦±£³ÖĖ®Ę½£¬¶ĮŹżĪŖ9.8mL”£µ¹³ö²æ·ÖŅŗĢåŗó£¬ø©ŹÓ°¼ŅŗĆęµÄ×īµĶ“¦£¬¶ĮŹżĪŖ3.5mL£¬ŌņøĆѧɜŹµ¼Źµ¹³öŅŗĢåµÄĢå»ż
A£®“óÓŚ6.3mL B£®Š”ÓŚ6.3mL C£®µČÓŚ6.3mL D£®ĪŽ·ØČ·¶Ø
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ėĀŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ”£Ä³Ģ½¾æŠ”×éĄūÓĆĻĀ
ĮŠ·“Ó¦ÖĘČ”Ė®ŗĻėĀ£ØN2H4·H2O£©”£
CO(NH2)2+ 2NaOH + NaClO = Na2CO3 + N2H4·H2O + NaCl
ŹµŃéŅ»£ŗ ÖʱøNaClOČÜŅŗ”££ØŹµŃé×°ÖĆČēÓŅĶ¼ĖłŹ¾£©
£Ø1£©ÅäÖĘ30%NaOHČÜŅŗŹ±£¬ĖłŠč²£Į§ŅĒĘ÷³żĮæĶ²Ķā»¹ÓŠ £ØĢī±źŗÅ£©”£
A£®ČŻĮæĘæ B£®ÉÕ± C£®ÉÕĘæ D£®²£Į§°ō
£Ø2£© ׶ŠĪĘæÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ ”£

£Ø3£© ŅņŗóŠųŹµŃéŠčŅŖ£¬ŠčĄūÓĆÖŠŗĶµĪ¶ØŌĄķ²ā¶Ø·“Ó¦ŗó׶ŠĪĘæÖŠ»ģŗĻČÜŅŗµÄNaOHµÄÅØ
¶Č”£ĒėŃ”ÓĆĖłĢį¹©µÄŹŌ¼Į(H2O2ČÜŅŗ”¢FeCl2ČÜŅŗ”¢0.1000mol·L-1ŃĪĖį”¢·ÓĢŖŹŌŅŗ)£¬Éč¼ĘŹµŃé·½°ø”£
ӣ
ŹµŃ鶞£ŗ ÖĘČ”Ė®ŗĻėĀ”££ØŹµŃé×°ÖĆČēÓŅĶ¼ĖłŹ¾£©

æŲÖĘ·“Ó¦ĪĀ¶Č£¬½«·ÖŅŗĀ©¶·ÖŠČÜŅŗ»ŗĀżµĪČėČż¾±ÉÕĘæÖŠ£¬³ä·Ö·“Ó¦”£
¼ÓČČÕōĮóČż¾±ÉÕĘæÄŚµÄČÜŅŗ£¬ŹÕ¼Æ108~114”ęĮó·Ö”££ØŅŃÖŖ£ŗN2H4·H2O + 2NaClO £½ N2”ü + 3H2O + 2NaCl£©
£Ø4£©·ÖŅŗĀ©¶·ÖŠµÄČÜŅŗŹĒ £ØĢī±źŗÅ£©”£
A£®CO (NH2) 2ČÜŅŗ B£®NaOHŗĶNaClO»ģŗĻČÜŅŗ
Ń”ŌńµÄĄķÓÉŹĒ ”£
ŹµŃéČż£ŗ ²ā¶ØĮó·ÖÖŠėĀŗ¬Į攣
³ĘČ”Įó·Ö5.000g£¬¼ÓČėŹŹĮæNaHCO3¹ĢĢ壬¼ÓĖ®Åä³É250mLČÜŅŗ£¬ŅĘ³ö25.00mL£¬ÓĆ0.1000mol·L-1µÄI2ČÜŅŗµĪ¶Ø”£µĪ¶Ø¹ż³ĢÖŠ£¬ČÜŅŗµÄpH±£³ÖŌŚ6.5×óÓŅ”££ØŅŃÖŖ£ŗN2H4·H2O + 2I2 = N2”ü+ 4HI + H2O£©
£Ø5£©µĪ¶Ø¹ż³ĢÖŠ£¬NaHCO3ÄÜæŲÖĘČÜŅŗµÄpHŌŚ6.5×óÓŅ£¬ŌŅņŹĒ ”£
£Ø6£©ŹµŃé²āµĆĻūŗÄI2ČÜŅŗµÄĘ½¾łÖµĪŖ18.00mL£¬Įó·ÖÖŠĖ®ŗĻėĀ£ØN2H4·H2O£©µÄÖŹĮæ·ÖŹżĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¼ģŃ黚²ńĶ·ÖŠŗ¬ÓŠµÄĀČ
ŌŖĖŲ£¬ĻČ½«»š²ńĶ·½žĆ»ÓŚÉŁĮæĖ®ÖŠ£¬Č”Ęä½žČ”Ņŗ£¬ĘäŗóµÄ²Ł×÷ÕżČ·µÄŹĒ
A£®µĪ¼ÓAgNO3ČÜŅŗ£¬¹Ū²ģŹĒ·ńÓŠ°×É«³Įµķ
B£®µĪ¼ÓAgNO3ČÜŅŗŗĶĻ”ĻõĖį£¬¹Ū²ģŹĒ·ńÓŠ°×É«³Įµķ
C£®µĪ¼ÓAgNO3ČÜŅŗ”¢Ļ”ĻõĖįŗĶNaNO2ČÜŅŗ£¬¹Ū²ģŹĒ·ńÓŠ°×É«³Įµķ
D£® µĪ¼ÓNaOHČÜŅŗ£¬¼ÓČČ£¬ŌŁÓĆĻ”ĻõĖįĖį»Æŗ󣬵ĪČėAgNO3ČÜŅŗ¹Ū²ģŹĒ·ńÓŠ°×É«³Įµķ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠŹµŃé¹ż³ĢÖŠµÄĻÖĻó¼°½įĀŪ¾łÕżČ·ĒŅ“ęŌŚŅņ¹ū¹ŲĻµµÄŹĒ

| ŹµŃé | ŹµŃéĻÖĻó | ½įĀŪ |
| A | ¹ćæŚĘæÖŠ¹āĮĮµÄĢś¶¤·ÅÖĆŅ»¶ĪŹ±¼äŗóÉśŠā | Ģś¶¤·¢ÉśĪöĒāøÆŹ“ |
| B | ×óÉÕ±ĀĮ±ķĆęĆ°ĘųÅŻ£¬ÓŅÉÕ±Ķ±ķĆęĆ°ĘųÅŻ | »ī¶ÆŠŌ£ŗAl£¾Fe£¾Cu |
| C | ×óÉÕ±ĘųĢåŃÕÉ«¼ÓÉī£¬ÓŅÉÕ±ĘųĢåŃÕÉ«±äĒ³ | NO2×Ŗ»ÆĪŖN2O4ĪüČČ |
| D | °×É«¹ĢĢåĻȱäĪŖ»ĘÉ«£¬ŗó±äĪŖŗŚÉ« | Ksp£ŗAgCl£¾AgI£¾Ag2S |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Ēė½«ŅŌĻĀ²ÄĮĻÓėÓ¦ÓĆĮģÓņ½ØĮ¢ĻąÓ¦µÄĮ¬Ļߣŗ
A£®ĀĮŗĻ½š(½šŹō²ÄĮĻ)”””””””””””””” a£®ŗ½Ģģ·É»śøōČČĶß
B£®Ģ¼ĻĖĪ¬ŌöĒæµÄŹ÷Ö¬»łø“ŗĻ²ÄĮĻ b£®ÖĘĆÅ“°æņ”¢ĒņÅÄ
C£®Ģ¼ĻĖĪ¬ŌöĒæµÄ½šŹō»łø“ŗĻ²ÄĮĻ c£®ÖĘ·É»ś»śŅķ
D£®Si3N4ĢÕ“ÉĪŖ»łĢåµÄĢ¼ d£®ÖĘĒņÅĵČĢåÓżÓĆĘ·
””ĻĖĪ¬ŌöĒæø“ŗĻ²ÄĮĻ ”” ¼°ČĖĢåČĶ“ų
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com