
| A. | 烷烃的通式为CnH2n+2,随n值增大,碳元素的质量百分含量逐渐减小 | |
| B. | 乙烯与溴发生加成反应的产物为溴乙烷 | |
| C. | 1 mol 苯恰好与3 mol氢气完全加成,说明一个苯分子中有三个碳碳双键 | |
| D. | n=7,主链上有5个碳原子烷烃共有五种 |
分析 A.烷烃的通式为CnH2n+2,C元素的质量分数为$\frac{12n}{14n+2}$=$\frac{12}{14+\frac{2}{n}}$;
B.乙烯中含碳碳双键,与溴发生加成反应;
C.苯中不含碳碳双键;
D.n=7,主链上有5个碳原子的烷烃,支链为2个甲基或1个乙基,可以看作取代戊烷形成的物质.
解答 解:A.烷烃的通式为CnH2n+2,C元素的质量分数为$\frac{12n}{14n+2}$=$\frac{12}{14+\frac{2}{n}}$,则随n值增大,碳元素的质量百分含量逐渐增大,故A错误;
B.乙烯中含碳碳双键,可与溴水发生加成反应生成1,2-二溴乙烷,故B错误;
C.苯中不含碳碳双键,但1 mol摩尔苯恰好与3摩尔氢气完全加成,故C错误;
D.n=7,主链上有5个碳原子的烷烃,支链为2个甲基或1个乙基,符合的有(CH3)3CCH2CH2CH3、CH3CH2C(CH3)2CH2CH3、CH3CH2CH(CH2CH3)CH2CH3、(CH3)2CHCH2CH(CH3)2、(CH3)2CHCH(CH3)CH2CH3,共5种,故D正确;
故选D.
点评 本题考查有机物的结构与性质,选项D为解答的易错点,注意减链法书写同分异构体,注重基础知识的考查,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 强酸性溶液中:K+、Fe2+、Cl-、NO3- | |
| B. | 强碱溶液中:Na+、K+、[Al(OH)4]-、CO32- | |
| C. | 强碱性溶液中:NH4+、Al3+、SO42-、NO3- | |
| D. | 含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③正确 | B. | ①②⑤正确 | C. | 都正确 | D. | ②③④⑤正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
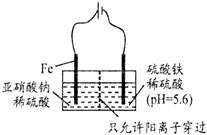 利用15N可以测定亚硝酸盐对地下水质的污染情况.
利用15N可以测定亚硝酸盐对地下水质的污染情况.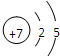 ,15N2的结构式为15N≡15N;
,15N2的结构式为15N≡15N;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
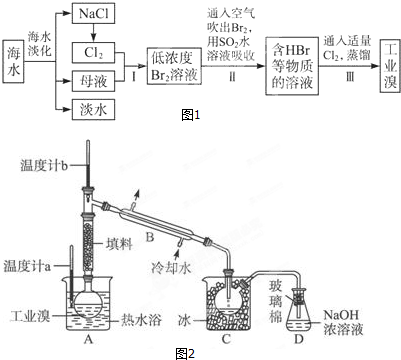
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
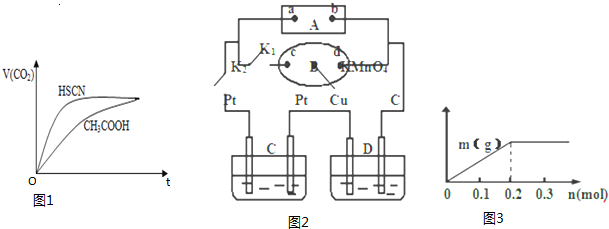
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 相关信息 |
| X | X的最高价氧化物对应的水化物化学式为H2XO3 |
| Y | Y是地壳中含量最高的元素 |
| Z | Z的基态原子最外层电子排布式为3s23p1 |
| W | W的一种核素的质量数为28,中子数为14 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度,可以加快反应速率 | |
| B. | 使用催化剂是为了加快反应速率 | |
| C. | 在上述条件下,SO2不能完全转化为SO3 | |
| D. | 达到平衡时,SO2的浓度与SO3的浓度一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
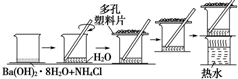 研究化学反应中的能量变化时,在一只小烧杯里,加入20g已研磨成粉末的Ba(OH)2•8H2O,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯中加入约10g NH4Cl晶体,根据下图所示实验步骤进行操作.回答下列问题:
研究化学反应中的能量变化时,在一只小烧杯里,加入20g已研磨成粉末的Ba(OH)2•8H2O,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯中加入约10g NH4Cl晶体,根据下图所示实验步骤进行操作.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com