
| A. | v(NH3)=0.2 mol•L-1•s-1 | B. | v(N2)=0.2 mol•L-1•min-1 | ||
| C. | v(H2)=0.2 mol•L-1•min-1 | D. | v(H2)=0.3 mol•L-1•min-1 |
分析 根据v=$\frac{△c}{△t}$计算v(NH3),再根据速率之比等于化学计量数之比计算v(N2)和v(H2).
解答 解:v(NH3)=$\frac{1mol•L{\;}^{-1}}{5min}$=0.2mol•L-1•min-1=12mol•L-1•s-1,
速率之比等于化学计量数之比,所以v(N2)=$\frac{1}{2}$v(NH3)=$\frac{1}{2}$×0.2mol•L-1•min-1=0.1mol•L-1•min-1,
v(H2)=$\frac{3}{2}$v(NH3)=$\frac{3}{2}$×0.2mol•L-1•min-1=0.3mol•L-1•min-1,所以ABC错误,故D正确.
故选:D.
点评 本题主要考查化学反应速率的计算,难度较小,化学反应速率计算可用定义法,也可用化学计量数法,本题两种方法同时运用,根据情况选择合适的方法.


科目:高中化学 来源: 题型:选择题
| A. | ① | B. | ①③ | C. | ②③④⑤⑥⑦ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
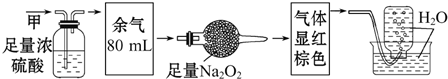
| A. | NH3、NO2、N2 | B. | NH3、NO、CO2 | C. | NH3、NO2、CO2 | D. | NO、CO2、N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 烧杯①中,若构成微型电池,负极反应式为2Al-6e-=2Al3+,正极反应式为 6H++6e-=3H2↑ | |
| B. | 烧杯①中,若将电解质溶液换成浓硝酸,构成微型电池时铝为负极,铜为正极 | |
| C. | 烧杯②中,若铁、铜构成微型电池,则铁为负极;若铝、铁构成微型电池,则铁为正极 | |
| D. | 烧杯②中,固体最终完全溶解,溶液呈蓝色.向溶液中滴加KSCN溶液,溶液不变色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
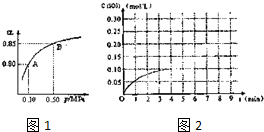
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

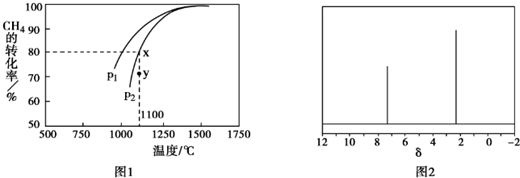
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量浓度均为1 mol•L-1的NaCl和MgCl2中:c(Cl-)=3c(Na+) | |
| B. | 等物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3•H2O,c(NH4+)由大到小的顺序是①>②>③>④ | |
| C. | 室温下,向0.01 mol•L-1 NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+) | |
| D. | 向0.2 mol•L-1 NaHCO3溶液中加入等体积0.1 mol•L-1 NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com