
【题目】反应:PCl5(g) ![]() PCl3(g)+Cl2(g)① 2HI(g)
PCl3(g)+Cl2(g)① 2HI(g) ![]() H2(g)+I2(g)② 2NO2(g)
H2(g)+I2(g)② 2NO2(g) ![]() N2O4(g)③在一定条件下,达到化学平衡时,反应物的转化率均是a%。若保持各自的温度不变、体积不变,分别再加入一定量的各自的反应物,则反应物的转化率( )
N2O4(g)③在一定条件下,达到化学平衡时,反应物的转化率均是a%。若保持各自的温度不变、体积不变,分别再加入一定量的各自的反应物,则反应物的转化率( )
A. 均不变 B. 均增大
C. ①增大,②不变,③减小 D. ①减小,②不变,③增大
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E 都含X元素,其转化关系如下图所示。

(1)请分别写出A、B、C、D、E的化学式(如为溶液请填溶质的化学式):
A _____,B _____,C ______,D_____,E___________。
(2)写出下列反应的化学方程式:
A+H2O:______________;
A+NaOH:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列五种有色溶液通入SO2时均能褪色或变色,其实质相同的是( ) ①品红溶液 ②酸性KMnO4溶液 ③滴有酚酞的NaOH溶液
④氯水 ⑤石蕊溶液.
A.①④
B.①③
C.①②⑤
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.硫元素的不同单质S2与S8互为同素异形体B.35Cl2和37Cl2互为同位素
C.(CH3)2CHCH3和CH3(CH2)2CH3互为同分异构体D.甲苯和间二甲苯互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由P、S、Cl、Ni等元素组成的新型材料有着广泛的用途,回答下列问题。
(1)基态 Cl原子核外电子排布式__________________________,P、S、Cl的第一电离能由大到小顺序
为____________________。
(2)SCl2分子中的中心原子杂化轨道类型是_____________,该分子构型为__________。
(3)Ni与CO能形成配合物Ni(CO)4,该分子中σ键与π键个数比为__________。
(4)已知MgO与NiO的晶体结构(如图1)相同,其中Mg2+和Ni2+的离子半径分别为66 pm和69 pm。则熔点:MgO_____NiO(填“>”、“<”或“=”),理由是_____________。
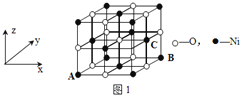
(5)若NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为______。
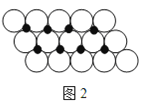
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+ 填充其中(如图2),已知O2-的半径为a m,每平方米面积上分散的该晶体的质量为______g。(用a、NA表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】100℃时,将0.1 mol N2O4置于1 L密闭的烧瓶中,然后将烧瓶放入100℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) ![]() 2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到反应限度的是( )
2NO2 (g)。下列结论不能说明上述反应在该条件下已经达到反应限度的是( )
①N2O4的消耗速率与NO2的生成速率之比为1∶2;②NO2的生成速率与NO2消耗速率相等;③烧瓶内气体的压强不再变化;④烧瓶内气体的质量不再变化;⑤NO2的物质的量浓度不再改变;⑥烧瓶内气体的颜色不再加深;⑦烧瓶内气体的平均相对分子质量不再变化;⑧烧瓶内气体的密度不再变化。
A. ②③⑥⑦ B. ①④⑧
C. 只有①④ D. 只有⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2的防治与利用对于环境保护意义重大。某小组在实验室中对SO2的性质及回收利用等相关问题进行探究。
(1)用下图装置制备纯净的SO2,发生装置中反应的化学方程式为________,装置的连接顺序为:a→________(按气流方向,用小写字母表示)
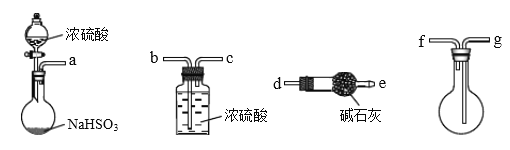
(2)用如图装置探究SO2的性质。限选试剂:NaOH溶液、稀H2SO4、H2O2溶液、FeCl3溶液、 淀粉-KI溶液、新制H2S溶液。

操作步骤 | 实验现象 | 解释原因 |
用注射器将新制H2S溶液注入充满SO2的烧瓶 | 产生乳白色浑浊 | +4价S有_______性 |
用注射器将_______溶液注入充满SO2的烧瓶 | _______ | +4价S有还原性,反应的离子方程式为_______ |
(3)工业上回收利用SO2的一种途径是:
![]()
该小组在实验室探究步骤Ⅱ时,一定条件下向100mL c0mol·L-1的(NH4)2SO3溶液通入空气后,欲测定溶液中(NH4)2SO3的氧化率(α)。
①为该小组设计实验方案(不必描述操作过程的细节,物理量的数值用字母表示):______________________________________________________________________________
②α =________×100%(用实验方案中的物理量表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。

(1)写出装置甲的电解总反应方程式________________________________________。
(2)为完成上述实验,正确的连接顺序为E→_________________(填写连接的字母)。
(3)对硬质玻璃管里的氧化铜粉末进行加热前,需要先通一段时间某气体并检验该气体的纯度,检验该气体已经纯的具体的操作和现象为_______________________________。
(4)乙装置的a瓶溶液可选用__________________。
A.淀粉碘化钾溶液 B.酸性高锰酸钾溶液 C.硫化钠溶液 D.Fe(NO3)2溶液
(5)若a瓶中盛放过量的NaHSO3溶液,写出发生的离子反应方程式_____________________。
(6)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案。精确测量硬质玻璃管的质量为a g,加入CuO后,精确测量硬质玻璃管和CuO的总质量为b g , 实验完毕后:
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g, 进而确定Cu的相对原子质量。
乙方案:通过精确测定生成水的质量d g,进而确定Cu的相对原子质量。
乙方案不足之处是________________________________________________________。
按甲方案进行计算,Cu的相对原子质量为__________。(用含a、b、c的式子来表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com