
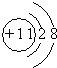 ;
;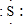 ,E离子的符号为Cl-;
,E离子的符号为Cl-;分析 A、B、C、D、E五种短周期元素,它们的原子序数依次增大,D的氢化物的分子式为H2D,D的最高价氧化物的化学式为DO3,D的最高价氧化物的中D的质量分数为40%,令D的相对原子质量为x,则$\frac{x}{x+48}$=40%,解得x=32,D原子的原子核中质子数和中子数相等,所以D元素原子的质子数为16,故D为硫元素;E原子的M电子层上共有7个电子,则E为氯元素;C单质在加热条件下与B单质反应生成淡黄色固体,该淡黄色固体可能为过氧化钠,故可能B为氧元素,C为钠元素,B的阴离子与C的阳离子和氖原子的电子层结构相同,常温常压下,B单质是气体,0.1mol的B单质与H2完全反应需2.408×1023个氢原子,经验证符合,故B为氧元素,C为钠元素;A原子最外电子层上有4个电子,原子序数最小,故A为碳元素,结合物质性质与元素周期律解答.
解答 解:A、B、C、D、E五种短周期元素,它们的原子序数依次增大,D的氢化物的分子式为H2D,D的最高价氧化物的化学式为DO3,D的最高价氧化物的中D的质量分数为40%,令D的相对原子质量为x,则$\frac{x}{x+48}$=40%,解得x=32,D原子的原子核中质子数和中子数相等,所以D元素原子的质子数为16,故D为硫元素;E原子的M电子层上共有7个电子,则E为氯元素;C单质在加热条件下与B单质反应生成淡黄色固体,该淡黄色固体可能为过氧化钠,故可能B为氧元素,C为钠元素,B的阴离子与C的阳离子和氖原子的电子层结构相同,常温常压下,B单质是气体,0.1mol的B单质与H2完全反应需2.408×1023个氢原子,经验证符合,故B为氧元素,C为钠元素;A原子最外电子层上有4个电子,原子序数最小,故A为碳元素.
(1)A为碳元素,位于元素周期表中第二周期IVA族,C的阳离子为Na+,离子结构示意图为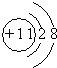 ,故答案为:第二周期IVA族;
,故答案为:第二周期IVA族;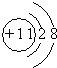 ;
;
(2)D为S元素,原子的电子式为 ,E为Cl,离子的符号为Cl-,故答案为:
,E为Cl,离子的符号为Cl-,故答案为: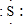 ;Cl-;
;Cl-;
(3)C单质和B单质在加热条件下生成化合物Na2O2,反应的化学方程式为2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2,Na2O2中所含化学键的类型是:离子键、共价键,Na2O2在生产生活中的一种应用:用于防毒面具等的供氧剂,
故答案为:2Na+O2$\frac{\underline{\;\;△\;\;}}{\;}$Na2O2;离子键、共价键;用于防毒面具等的供氧剂;
(4)C与E形成化合物为NaCl,电解NaCl的水溶液的离子方程式为:2Cl-+2 H2O $\frac{\underline{\;电解\;}}{\;}$ 2 OH-+H2↑+Cl2↑,
故答案为:2Cl-+2 H2O $\frac{\underline{\;电解\;}}{\;}$ 2 OH-+H2↑+Cl2↑;
(5)由于氯元素的非金属性比硫强,则最高价氧化物对应水化物的酸性强弱:H2SO4<HClO4,气态氢化物的稳定性:H2S<HCl,
故答案为:H2SO4<HClO4;H2S<HCl;氯元素的非金属性比硫强.
点评 本题考查考查结构性质位置关系应用、常用化学用语、元素周期律等,推断元素是解题关键,侧重于对基础知识的综合应用的考查,注意对元素周期律的理解与应用,难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 当△H为“-”时,表示该反应为吸热反应 | |
| B. | 化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关 | |
| C. | H2S的燃烧热△H=-a kJ•mol-1,则表示H2S燃烧热的热化学方程式为2H2S(g)+3O2(g)═2SO2(g)+2H2O(l)△H=-2a kJ•mol-1 | |
| D. | 反应热的大小与反应物所具有的能量和生成物所具有的能量无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
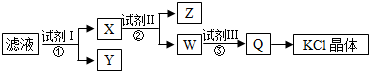
| A. | 图示的步骤中必需要经过2次过滤操作 | |
| B. | 起始滤液呈中性 | |
| C. | 试剂Ⅱ为Na2CO3溶液 | |
| D. | 试剂Ⅲ为盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
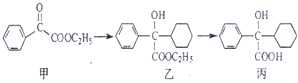
| A. | 化合物甲中的含氧官能团有 羰基和酯基 | |
| B. | 化合物乙与NaOH水溶液在加热条件下反应可生成化合物丙 | |
| C. | 化合物乙中含有1个手性碳原子 | |
| D. | 在NaOH醇溶液中加热,化合物丙可发生消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 陶瓷、水晶、水泥、玻璃都属于硅酸盐 | |
| B. | 水玻璃是纯净物,可用于生产黏合剂和防火剂 | |
| C. | 某硅酸盐的化学式为KAlSi3O8,可用K2O.Al2 O3.6SiO2表示 | |
| D. | 高纯硅可用于制造光导纤维,高纯二氧化硅可用于制造太阳能电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 过氧化钠与二氧化碳反应中电子转移数为0.2NA | |
| B. | 一定量的C02为0.1NA | |
| C. | 18.4g固体物质为0.lmol Na2C03和0.05molNa202的混合物 | |
| D. | 一定量的Na202为0.lmol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等PH的氨水、KOH溶液、Ba(OH)2溶液中:c(NH4+)=c(K+)=c(Ba2+) | |
| B. | 等体积、等物质的量浓度的NaCl和NaClO溶液中离子总数(N):N(NaCl)<N(NaClO) | |
| C. | 将10mol0.1mol•L-1Na2CO3溶液逐渐滴加到10mL0.1mol•L-1盐酸中:c(Na+)>c(Cl-)>c(HCO3-)>c(CO32-) | |
| D. | 室温下,向0.1mol•L-1的醋酸钠溶液中通入氯化氢气体,使溶液的pH=7:>c(CH3COOH)=c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若HA 的电离能力大于A-的水解能力,则有c(A-)>c(Na+)>c(HA)>c(H+)>c(OH-) | |
| B. | 若A-的水解能力大于HA 的电离能力,则有c(Na+)>c(HA)>c(A-)>c(OH-)>c(H+) | |
| C. | 无论该溶液呈酸性还是碱性,都有 c(Na+)+c(H+)=c(A-)+c(OH-) | |
| D. | 无论该溶液呈酸性还是碱性,都有2c(Na+)=c(A-)+c(HA) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com