
【题目】对醋酸的电离平衡不产生影响的微粒是( )
A.![]()
B.HBr
C.
D.HCHHCOO﹣
【答案】C
【解析】解:A.电子式 ![]() 表示的为水,加水稀释,醋酸的电离程度增大,故A不选;B.加入HBr,溶液中氢离子浓度增大,抑制了醋酸的电离,故B不选;
表示的为水,加水稀释,醋酸的电离程度增大,故A不选;B.加入HBr,溶液中氢离子浓度增大,抑制了醋酸的电离,故B不选;
C.  为钾离子,加入钾离子对醋酸的电离平衡无影响,故C选;
为钾离子,加入钾离子对醋酸的电离平衡无影响,故C选;
D. 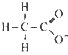 为醋酸根离子,加入醋酸根离子,溶液中醋酸根离子浓度增大,抑制了醋酸电离,故D不选;
为醋酸根离子,加入醋酸根离子,溶液中醋酸根离子浓度增大,抑制了醋酸电离,故D不选;
故选C.
【考点精析】根据题目的已知条件,利用弱电解质在水溶液中的电离平衡的相关知识可以得到问题的答案,需要掌握当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.


科目:高中化学 来源: 题型:
【题目】将下列各组物质按酸、碱、盐分类顺序排列,正确的是
A. 硫酸,纯碱,石灰石B. 醋酸,烧碱,硫酸铜
C. 磷酸,熟石灰,苛性钾D. 醋酸,小苏打,熟石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某未知溶液中加入硝酸银溶液有白色沉淀生成,加入稀硝酸后,沉淀部分溶解,有无色无味的气体生成,将气体通入澄清石灰水中,石灰石变浑浊,由此判断该溶液中含有
A. Cl- SO42-B. Cl- NO3-C. Cl- CO32- D. Cl- OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于a g 氢气 和b g氦气,下列说法正确的是( )
A. 同温、同压下,氢气和氦气的体积比是a:2b
B. 同温、同压下,若a=b,则氢气 和氦气的物质的量之比为2:1
C. 体积相同时,氦气的质量一定大于氢气的质量
D. 同温同压下,若二者的物质的量相同,其所含原子数也相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I 下列九种物质:①稀硝酸 ②CO ③NH3·H2O ④熔融NaHSO4⑤CaO ⑥Cu ⑦蔗糖⑧Fe2(SO4)3⑨酒精
(1)用序号填空: 属于电解质的是 __________ ;能导电的是_______________ ;
(2)写出④、⑧两种物质在水溶液中的电离方程式:
④______________________________;⑧__________________________________________ 。
II (1)画出S2-的结构示意图_______________________。
(2)质量数为A、中子数为N的离子R2+,该离子的核外电子数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家说:“没有碳,就没有生命。”以下说法不正确的是
A. 地球上的生命是在碳元素的基础上建立起来的
B. 碳是构成细胞的最基本元素
C. 碳元素是各种大分子化合物中含量最多的元素
D. 生物大分子以碳链为骨架
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性溶液中能大量共存而且为无色透明的溶液是
A. NH4+,Al3+,SO42-,NO3-
B. K+,Na+,NO3-,CO32-,
C. K+,MnO4-,NH4+,NO3-
D. Na+,K+,HCO3-,NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,将一定量的冰醋酸加水稀释,稀释过程中溶液的导电性变化如图所示.
则下列说法错误的是( )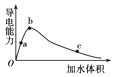
A.醋酸的电离程度:a<b<c
B.溶液的pH值:b<a<c
C.蘸取a点溶液滴在湿润的pH试纸上,测得pH值一定偏大
D.若分别取a、b、c三点的溶液各10 mL,各用同浓度的氢氧化钠溶液中和,消耗NaOH溶液的体积a>b>c
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是化合物,B是金属单质,它们之间相互反应以及生成物之间的转化关系如图所示: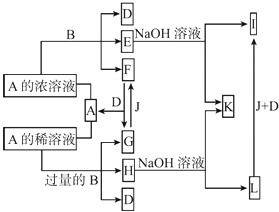
(1)金属B在元素周期表中的位置是 , B和A的浓溶液反应的条件是 . 写出少量B与A的稀溶液反应的离子方程式: .
(2)常温下0.1 mol/L E的水溶液中各离子浓度大小关系为 .
(3)L转化为I的现象是 . 写出有关的化学方程式: .
(4)如何检测H溶液中阳离子的存在,写出实验操作方法、现象、结论: .
(5)已知25℃时Fe(OH)3的Ksp=3.5×10﹣39 , 现将4.0×10﹣8 mol/L E溶液与2.0×10﹣8 mol/L NaOH溶液等体积混合(忽略溶液混合时体积的变化),通过列式计算说明是否有沉淀产生: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com