
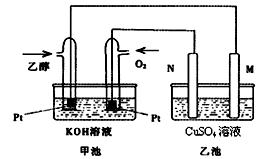
 下),理论上需通入乙醇 g?
下),理论上需通入乙醇 g? 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 Cl(aq) ΔH=-72.3 kJ·mol–1
Cl(aq) ΔH=-72.3 kJ·mol–1 HCl(aq) = NH4C1(aq) ΔH= -52.3 kJ·mol–1
HCl(aq) = NH4C1(aq) ΔH= -52.3 kJ·mol–1
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.碳和水反应吸收热量131.3 kJ |
| B.固体碳和气态水各1 mol反应,放出131.3 kJ的热量 |
| C.1 mol C跟1 mol H2O反应吸收131.3 kJ的热量 |
| D.1 mol C(s)和1 mol H2O(g)反应生成一氧化碳和氢气,并吸收131.3 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.放热反应 | B.吸热反应 | C.化合反应 | D.分解反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

A.焦炭在高温下与水蒸气的反应是吸热反应 | B.吸热反应一定是反应物总能量低于生成物总能量 | C.电能是经过一次能源加工转换得到的能源,因此,属于二次能源 | D.断开旧的化学键放出的能量与形成新化学键吸收的能量之差通常以热量的形式释放 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 温度/°C | 200 | 300 | 400 | 500 | 600 |
| 氨含量/% | 89.9 | 71.0 | 47.0 | 26.4 | 13.8 |

 2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)= ;该温度下的平衡常数K= (用分数表示);俗使K增大,可以采取的措施是 。
2NH3,2min达到平衡状态时,H2转化率是50%,则用H2表示该反应的平均速率v(H2)= ;该温度下的平衡常数K= (用分数表示);俗使K增大,可以采取的措施是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 则2Fe(s)+O2(g ) = Fe2O3(s) 的△H是
则2Fe(s)+O2(g ) = Fe2O3(s) 的△H是| A.-824.4kJ·mol-1 | B.-627.6kJ·mol-1 |
| C.-744.7kJ·mol-1 | D.-169.4kJ·mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.2SO2+O2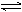 2SO3; △H=-196.6kJ/mol 2SO3; △H=-196.6kJ/mol |
| B.C(s)+O2(g)==CO2(g);△H=393.5kJ/mol |
| C.1/2H2(g)+1/2Cl2(g)==HCl(g);△H=-92.5kJ/mol |
| D.H+(aq)+OH-(aq)==H2O(l);△H=57.3kJ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com