
【题目】用18 mol·L-1 浓硫酸配制90 mL 3.0 mol·L-1 稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积
②量取一定体积的浓硫酸
③溶解
④
⑤转移、洗涤
⑥定容、摇匀
⑦装瓶贴标签
完成下列问题:
(1)所需浓硫酸的体积是_____________,量取浓硫酸所用的量筒的规格是 _____________(从下列中选用A.10 mL B.25 mL C.50 mL D.100 mL)。浓硫酸稀释的操作______________。
(2)第④步实验的操作是_______________________________________________________
(3)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)
A.用量筒量取浓硫酸后洗涤量筒并将洗涤液注入容量瓶内___________________;
B.容量瓶用蒸馏水洗涤后残留有少量的水________________;
C.所用过的烧杯、玻璃棒未洗涤________________;
D.定容时俯视刻度线________________。
【答案】16.7mL B将浓硫酸沿烧杯内壁缓慢倒入盛有蒸馏水的烧杯中,并用玻璃棒不断搅拌 冷却偏大无影响偏小偏大
【解析】
(1)根据“大而近”的原则,选用100mL容量瓶配制90mL溶液,根据c(浓溶液)V(浓溶液)=c(稀溶液)V(稀溶液)计算V(浓硫酸),由计算结果和“大而近”的原则选择量筒的规格。稀释浓硫酸应“酸入水中,并不断搅拌”。
(2)由浓溶液配制一定体积物质的量浓度稀溶液的实验步骤:计算→量取→稀释→冷却→转移→洗涤→定容→摇匀。
(3)根据公式cB=![]() 分析,操作失误使nB偏大或V(aq)偏小,会使所配溶液浓度偏大,反之偏小。
分析,操作失误使nB偏大或V(aq)偏小,会使所配溶液浓度偏大,反之偏小。
(1)根据“大而近”的原则,选用100mL容量瓶配制90mL溶液,根据c(浓溶液)V(浓溶液)=c(稀溶液)V(稀溶液),18mol/LV(浓硫酸)=3mol/L×0.1L,解得V(浓硫酸)=16.7mL;根据“大而近”的原则,应选用25mL规格的量筒,答案选B。稀释浓硫酸的操作是:将浓硫酸沿烧杯内壁缓慢倒入盛有蒸馏水的烧杯中,并用玻璃棒不断搅拌。
(2)由浓溶液配制一定体积物质的量浓度稀溶液的实验步骤:计算→量取→稀释→冷却→转移→洗涤→定容→摇匀。根据实验步骤,第④步实验的操作是:冷却。
(3)根据公式cB=![]() 分析。
分析。
A项,用量筒量取浓硫酸后洗涤量筒并将洗涤液注入容量瓶内,硫酸物质的量偏大,所配溶液的浓度偏大。
B项,容量瓶用蒸馏水洗涤后残留有少量的水,对所配溶液的溶质物质的量和溶液的体积均无影响,对所配溶液的浓度无影响。
C项,所用过的烧杯、玻璃棒未洗涤,溶质没有全部转移入容量瓶中,溶质物质的量偏小,所配溶液的浓度偏小。
D项,定容时俯视刻度线,所配溶液体积偏小,所配溶液浓度偏大。


科目:高中化学 来源: 题型:
【题目】为探究一溴环己烷(![]() )与NaOH的醇溶液共热发生的是水解反应还是消去反应,甲、乙、丙三位同学分别设计如下三个实验方案:
)与NaOH的醇溶液共热发生的是水解反应还是消去反应,甲、乙、丙三位同学分别设计如下三个实验方案:
甲:向反应混合液中滴入稀硝酸中和NaOH,然后再滴入AgNO3溶液,若有浅黄色沉淀生成则可证明发生了消去反应。
乙:向反应混合液中滴入溴水,若溶液颜色很快褪去,则可证明发生了消去反应。
丙:向反应混合液中滴入酸性KMnO4溶液,若溶液颜色变浅,则可证明发生了消去反应。
其中正确的是( )
A. 甲 B. 乙 C. 丙 D. 上述实验方案都不正确
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1) ______mol CO2中含有氧原子数跟1.806×1024个H2O分子含有的氧原子数相同。
(2)0.4 mol SiH4分子中所含原子数与________g HCl分子中所含原子数相等。
(3)标准状况下的甲烷和一氧化碳的混合气体8.96 L,其质量为7.60 g,则混合气体中甲烷的体积为____________;一氧化碳的质量为___________。
(4)等物质的量O2和臭氧(O3),其质量之比为______________。若O2和O3质量相等,则其原子数之比为_____________。
(5)含MgCl2、KCl、Na2SO4三种溶质的混合液中,已知其中含Cl-1.5 mol,K+和Na+共1.5 mol,Mg2+为0.5 mol,则SO42-的质量为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
Ⅰ.脱硝:已知:H2的燃烧热为285.8kJ/mol N2(g) +2O2(g) = 2NO2(g)△H = +133kJ/mol、H2O(g) = H2O(l) △H = -44kJ/mol。催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为_____________________。
Ⅱ.脱碳:向2L密闭容器中加入2molCO2、6molH2,在适当的催化剂作用下,发生反应:CO2(g) + 3H2(g) ![]() CH3OH(l) + H2O(l) △H < 0
CH3OH(l) + H2O(l) △H < 0
(1)①该反应自发进行的条件是__________(填“低温”、“高温”或“任意温度”),
②下列叙述能说明此反应达到平衡状态的是___________。
a.混合气体的平均式量保持不变 ;b.CO2和H2的体积分数保持不变;
c. CO2和H2的转化率相等 ;d.混合气体的密度保持不变
e.1molCO2生成的同时有3molH—H键断裂
③CO2的浓度随时间(0~t2)变化如图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t6内CO2的浓度随时间的变化_____。

(2)改变温度,使反应CO2(g) + 3H2(g) ![]() CH3OH(g) + H2O(g) △H < 0中的所有物质都为气态。起始温度体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
CH3OH(g) + H2O(g) △H < 0中的所有物质都为气态。起始温度体积相同(T1℃、2L密闭容器)。反应过程中部分数据见下表:
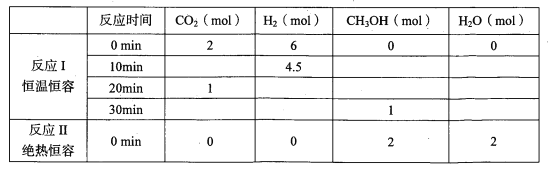
①达到平衡时,反应Ⅰ、Ⅱ对比:平衡常数K(I)_______K(II)(填“>”、“<”或“=”,下同);平衡时CH3OH的浓度c(I)_______c(II)。
②对反应Ⅰ,前10min内的平均反应速率v(CH3OH)=_______________。在其它条件不变下,若30min时只改变温度为T2 ℃,此时H2的物质的量为3.2mol,则T1______T2(填“>”、“<”或“=”)。若30min时向容器中再充入1molCO2和1molH2O(g),则平衡_________移动(填“正向”、“逆向”或“不”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列有关叙述错误的是
A. 80gCuO和Cu2S的混合物中,所含铜原子数为NA
B. 1molNaBH4与足量水反应(NaBH4+H2O=NaBO2+H2↑)时转移的电子数为:4NA
C. pH=13的Ba(OH)2溶液中,含有OH-0.2NA个
D. 密闭容器中PCl3与Cl2反应生成molPCl5(g),增加2A个P-C1键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将20.0 g 14%的NaCl溶液与30.0 g 24%的NaCl溶液混合,混合后得到密度为 1.17 g·cm-3的溶液。请计算:
(1)混合后的溶液中NaCl的质量分数是多少?___________
(2)混合后的溶液的物质的量浓度为多少?_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、有甲基、苯基、羟基、羧基四种基团,在它们两两组合形成的化合物中,写出具有以下性质的物质的结构简式:
(1)能使石蕊试液变色的有______种.
(2)催化氧化后产物能与新制氢氧化铜发生氧化还原反应的是______
(3)不同情况下与氢氧化钠反应能生成两种盐的是______.
II、有机物A可由葡萄糖发酵得到,也可从酸牛奶中提取.纯净的A为无色黏稠液体,易溶于水.为研究A的组成与结构,进行了如下实验:
实验步骤 | 解释或实验结论 |
(1)称取A 9.0 g,升温使其汽化,测其密度是相同条件下H2的45倍. | (1)A的相对分子质量为:________. |
(2)将此9.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g | (2)A的分子式为:________. |
(3)另取A 9.0 g,跟足量的NaHCO3粉末反应,生成2.24 L CO2(标准状况),若与足量金属钠反应则生成2.24 L H2(标准状况). | (3)用结构简式表示A中含有的官能团:________、________. |
(4)A的核磁共振氢谱如下图:
| (4)A中含有________种氢原子. |
(5)综上所述,A的结构简式________. | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com