
| A. | 1mol NH5中含有5NA个N-H键(NA为阿伏加德罗常数) | |
| B. | NH5中既有共价键,又有离子键 | |
| C. | NH5的电子式为: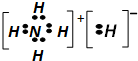 | |
| D. | 与水反应时,水作氧化剂,生成1mol氢气,转移2mol电子 |
分析 固体A的化学式为NH5,它的所有原子的最外层都符合相应稀有气体的最外电子层结构,则NH5属于铵盐,电子式为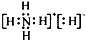 ,铵根离子和氢离子之间存在离子键,铵根离子中N原子和H原子之间存在共价键,NH5+H2O→NH3•H2O+H2↑,NH5中-1价H变为0,H2O中+1价的H变为O,据此分析解答.
,铵根离子和氢离子之间存在离子键,铵根离子中N原子和H原子之间存在共价键,NH5+H2O→NH3•H2O+H2↑,NH5中-1价H变为0,H2O中+1价的H变为O,据此分析解答.
解答 解:A.NH5中存在离子键和共价键,1 mol NH5中含有4NA个N-H键(NA表示阿伏加德罗常数),含有1mol离子键,故A错误;
B.NH5属于铵盐,铵根离子和氢离子之间存在离子键、铵根离子中N原子和H原子之间存在共价键,所以NH5中既有共价键又有离子键,故B正确;
C.NH5属于铵盐,铵根离子和氢离子之间存在离子键、铵根离子中N原子和H原子之间存在共价键,电子式为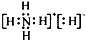 ,故C正确;
,故C正确;
D.NH5+H2O→NH3•H2O+H2↑,N元素的化合价均为-3价,NH5中-1价H变为0,H2O中+1价的H变为O,水是氧化剂,NH5是还原剂,生成1mol氢气,转移1mol电子,故D错误;
故选BC.
点评 本题考查物质结构和性质,侧重考查学生获取信息、加工信息能力,题目难度不大,明确该物质结构是解本题关键,注意该物质中存在的化学键,注意该物质中H元素化合价不都相等.


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2 L甲烷气体含有的甲烷分子数为0.5NA | |
| B. | 标准状况下,22.4 L氦气与22.4 L氮气所含原子数相同 | |
| C. | 标准状况下,11.2 L CO与N2的混合气体与11.2 L O2所含分子数相同,原子数也相同 | |
| D. | 标准状况下,22.4 L CCl4中含共价键数为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| Fe3+ | Fe2+ | Cu2+ | |
| 开始沉淀时的pH | 2.7 | 7.6 | 5.2 |
| 完全沉淀时的pH | 3.7 | 9.6 | 6.4 |
| 第一次实验 | 第二次实验 | |
| 坩埚质量(g) | 14.520 | 14.670 |
| 坩埚质量+晶体质量(g) | 17.020 | 18.350 |
| 第一次加热、冷却、称量(g) | 16.070 | 16.989 |
| 第二次加热、冷却、称量(g) | 16.070 | 16.988 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
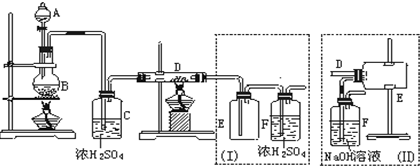
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
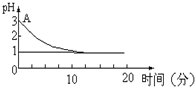 关于“电解氯化铜溶液时的pH值变化”问题,化学界有以下两种不同的观点:
关于“电解氯化铜溶液时的pH值变化”问题,化学界有以下两种不同的观点:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com