
【题目】下列关于乙烯和苯的叙述中,错误的是
A. 乙烯能使酸性高锰酸钾溶液褪色
B. 乙烯可以燃烧
C. 苯能使酸性高锰酸钾溶液褪色
D. 苯可以燃烧
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.非金属元素形成的化合物不可能是离子化合物
B.金属原子和非金属原子间也可形成共价键
C.离子化合物中可能含有共价键
D.共价化合物中不能含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案设计中,可行的是( )
A. 加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉
B. 用萃取的方法分离汽油和煤油
C. 用溶解、过滤的方法分离KNO3和NaCl固体的混合物
D. 将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是用98%的浓H2SO4(ρ=1.84 g·cm-3;物质的量浓度为18.4mol/L)配制0.5 mol·L-1的稀硫酸500 mL的实验操作,请按要求填空:
(1)所需浓硫酸的体积为________。
(2)如果实验室有10 mL、20 mL、50 mL的量筒,应选________的最好,量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将(填“偏高”、“偏低”或“无影响”)____________。
(3)将量取的浓硫酸沿烧杯内壁慢慢注入盛有约100 mL水的烧杯中,并不断搅拌,目
的是________________________。
(4)将冷却至室温的上述溶液沿________注入________中,并用50 mL蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液要转入到容量瓶中,并振荡。
(5)加水至距刻度线1 cm~2 cm处,改用________加水至刻度线,使溶液的________正好跟刻度线相平,把容量瓶塞好,反复颠倒振荡,摇匀溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的工业废水中含有大量的FeSO4 、较多的Cu2+ 、H+和少量的Na+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。其一种生产工艺如下:
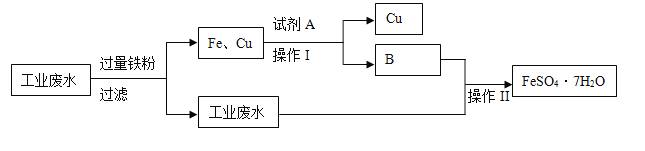
回答下列问题:
(1)写出工业废水中加入过量铁粉发生化学反应离子方程式,并用“单线桥”表示电子转
移方向和数目_________________________。
(2)试剂A化学式___________;生成物B化学式__________。
(3)操作I的名称________,操作II的名称______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气溶于水发生反应:Cl2 + H2O = HCl + HClO 。氯水中起杀菌消毒作用的是
A. Cl2B. H2OC. HClD. HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】提纯下列物质(括号内为少量杂质),所选用的除杂试剂与分离方法正确的是( )
不纯物质 | 除杂试剂 | 分离方法 | |
A | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 过滤 |
B | 乙烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
C | 苯(Br2) | KOH溶液 | 分液 |
D | 苯(苯酚) | 浓溴水 | 过滤 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮族元素和硼族元素在生产生活中有很重要的地位.
(1)写出硼族元素Ga的基态原子核外电子排布式
(2)NF3的分子构型为 , NO3﹣的空间构型为 , 1mol NO3﹣中含有的σ键的数目为: .
(3)氮化硼的立方结晶的变体被认为是已知的最硬的物质.BN的晶体结构与金刚石相似,其中B原子的杂化方式为
(4)元素第一电离能的大小:As(填“<”“>”或“=”)Ga,原因是 .
(5)相同条件下,在水中的溶解度:NH3(填“<”“>”或“=”)PH3 , 原因是 .
(6)已知立方砷化镓晶胞的结构如图所示,其晶胞边长为c pm.则砷化镓的化学式为 , 晶胞中As原子和它最近的Ga原子之间的距离为pm(用含c的式子表示),砷化镓的密度为gcm﹣3(设NA为阿伏伽德罗常数的值,用含c、NA的式子表示,原子量:Ga﹣70,As﹣75). 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】综合题。
(1)氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是
A.Cl2+2KBr═Br2+2KCl
B.2NaHCO3 ![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.4Fe(OH)2+O2+2H2O═4Fe(OH)3
D.CH4+2O2CO2+2H2O
(2)高锰酸钾和氢溴酸溶液可以发生如下反应:
2KMnO4+16HBr═5Br2+2MnBr2+2KBr+8H2O
①其中还原剂 , 还原产物是 .
②若消耗0.1mol氧化剂,则被氧化的还原剂的物质的量为 , 转移电子的物质的量是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com