
��1�� 20����30�����Eyring��Pzer����ײ���۵Ļ����������ѧ��Ӧ�Ĺ���̬���ۣ���ѧ��Ӧ������ͨ������ײ������ɵģ������ڷ�Ӧ�ﵽ������Ĺ����о���һ���������Ĺ���̬����ͼ��NO2��CO��Ӧ����CO2��NO�����е������仯ʾ��ͼ�� ˵�������Ӧ�� ������ȡ����ȡ�����Ӧ��NO2��CO�� ������ ������ڡ�����С�ڡ����ڡ���CO2��NO����������
˵�������Ӧ�� ������ȡ����ȡ�����Ӧ��NO2��CO�� ������ ������ڡ�����С�ڡ����ڡ���CO2��NO����������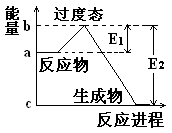
��2����ij���Ϊ2L���ܱ������г���1.5mol NO2��2mol CO����һ�������·�����Ӧ��NO2+CO CO2+NO��2 minʱ�����������NO�����ʵ���Ϊ0.5 mol ���ٴ˶�ʱ���ڣ���CO2��ʾ��ƽ����Ӧ����Ϊ ��2 minʱ������������������ʵ���Ϊ_________.
CO2+NO��2 minʱ�����������NO�����ʵ���Ϊ0.5 mol ���ٴ˶�ʱ���ڣ���CO2��ʾ��ƽ����Ӧ����Ϊ ��2 minʱ������������������ʵ���Ϊ_________.
��1�� ���� ����
��2��0.125mol/Lmin 3.5mol
���������������1����Ӧ������������������������������˸÷�Ӧʱ���ȷ�Ӧ�����Է�Ӧ�����������һ����̼�����������ڲ��������̼��һ������������������2������������һ������������Ϊ0.5����2�ٳ���2����0.125 mol/Lmin����ѧ����֮�ȵ��ڻ�ѧ������֮�ȣ���һ����̼��һ�������Ļ�ѧ��������Ϊ1��1���ԣ�������̼������Ϊ0.125mol/Lmin ��NO2+CO CO2+NO��2 min������0.5Ħ����һ����������Ҳ������0.5Ħ���Ķ�����̼��ͬʱҲ������0.5Ħ����һ����̼�Ͷ�������������ʣ���һ����̼Ϊ2��ȥ0.5����1.5��ʣ��Ķ�������Ϊ1.5��ȥ0.5����1Ħ������������������������ʵ���Ϊ1.5+1+0.5+0.5����3.5Ħ��
CO2+NO��2 min������0.5Ħ����һ����������Ҳ������0.5Ħ���Ķ�����̼��ͬʱҲ������0.5Ħ����һ����̼�Ͷ�������������ʣ���һ����̼Ϊ2��ȥ0.5����1.5��ʣ��Ķ�������Ϊ1.5��ȥ0.5����1Ħ������������������������ʵ���Ϊ1.5+1+0.5+0.5����3.5Ħ��
���㣺���黯ѧ��Ӧ�������Լ���ѧ��Ӧ���ʵ����֪ʶ



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪��2H2(g)��O2(g)=2H2O(l) ��H����571.6 kJ/mol������������ȷ����( )
| A��2������Ӻ�1�������ӷ�Ӧ����2��ˮ���ӣ��ų�����571.6 kJ |
| B��2 mol H2(g)��1 mol O2(g)��Ӧ����2 mol H2O(l)����������571.6 kJ |
| C��2 mol H2O(l)�ֽ�Ϊ2 mol H2(g)��1 mol O2(g)����������571.6 kJ |
| D��2 mol H2(g)��1 mol O2(g)��Ӧ����2 mol H2O(g)���ų�����571.6 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���淴ӦA+B(s) C�ﵽƽ������ۼ�ѹ����,B��ת���ʶ����������н�����ȷ���ǣ� ��
C�ﵽƽ������ۼ�ѹ����,B��ת���ʶ����������н�����ȷ���ǣ� ��
A. AΪ���壬CΪ���壬����ӦΪ���ȷ�Ӧ
B. AΪ���壬CΪ���壬����ӦΪ���ȷ�Ӧ
C. AΪ���壬CΪ���壬����ӦΪ���ȷ�Ӧ
D. A��C��Ϊ���壬����ӦΪ���ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��12�֣���1���̲��ں��ġ���ȼ�����Ǹ�ѹ���γɵ��������ļ���ˮ������壨����ʽΪCH4��9H2O������356g����ȼ�����ͷų��ļ���ȼ�գ�����Һ̬ˮʱ�ܷų�1780.6 kJ�������������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��_______________________________��
��2�� ��100��ʱ����0��100mol��N2O4�������1 L���ݳ�յ��ܱ������У���һ��ʱ��Ը����������ʵ�Ũ�Ƚ��з����õ��±����ݣ�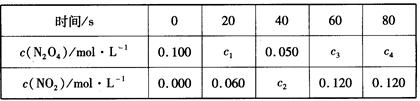
�ٴӱ��з������÷�Ӧ��ƽ�ⳣ��Ϊ___________��
�������������£�60s��N2O4��ƽ����Ӧ����Ϊ_____________��
�۴�ƽ������������ĸı��ʹNO2Ũ���������_________��
| A�������������ݻ� | B���ٳ���һ������N2O4 |
| C���ٳ���һ������NO2 | D���ٳ���һ������He |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ�ſ��ܷ�����ѧ��Ӧ����Щ���ӱ���Ϊ����ӡ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λͨ����kJ��mol��1��ʾ��
������۲���ͼ��Ȼ��ش����⡣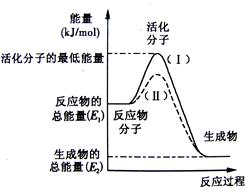
��1��ͼ����ʾ��Ӧ�� (����ȡ����ȡ�)��Ӧ�������÷�Ӧʱ (���Ҫ������Ҫ��)���ȣ��÷�Ӧ����ЧӦ�ľ���ֵΪ
(�ú�E1��E2�Ĵ���ʽ��ʾ)��
��2����֪��Ӧ��H2(g)��1/2 O2(g)��H2O(g)����ЧӦΪΪ241.8 kJ��mol��1�������淴Ӧ�Ļ��Ϊ_____kJ��mol��1��
��3������ͬһ��Ӧ��ͼ������(��)��ʵ��(��)��ȣ���ܴ�ͣ�����Ӱٷ������࣬��Ӧ���ʼӿ죬����Ϊ����ܵ�ԭ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��3�֣����·�Ӧ����ľ̿��ˮ�Ʊ�ˮú�� ������طֽ� ��ըҩ��ը ���������кͷ�Ӧ ����ʯ����ˮ��������ʯ�� �� Ba(OH)2��8H2O��NH4Cl ����̬ˮҺ�������ڷ��ȷ�Ӧ����
������ţ���д����Ӧ�Ļ�ѧ����ʽ__ ____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
(8��)�״���һ������ȼ�ϣ�������ȼ�ϵ�ء�
��1����ҵ�Ͽ����������ַ�Ӧ�Ʊ��״���
��CO(g) + 2H2(g)  CH3OH(g) ��H1 ��CO2(g)��3H2(g)
CH3OH(g) ��H1 ��CO2(g)��3H2(g) CH3OH(g) + H2O(g) ��H2
CH3OH(g) + H2O(g) ��H2
��֪����2H2(g)+ O2(g) �� 2H2O(g) ��H3����2CO(g)��O2(g)��2CO2(g) �ķ�Ӧ��
��H��______���æ�H1����H2����H3��ʾ����
��2�������״���ԭ��CO��H2��Դ�ڣ�CH4(g) + H2O(g)  CO(g) + 3H2(g) ��H4��
CO(g) + 3H2(g) ��H4��
һ��������CH4��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼa����H4______0��P1_________P2
���<������>��������
ijʵ��С�������ͼb��ʾ�ļ״�ȼ�ϵ��װ�ã�����һ��ʱ�����Һ��PH (������ ��С������)�������ĵ缫��ӦʽΪ_______ ____��
��4����ͭ��������õ��Ĵ�ͭ������Fe��Ag��Au�Ƚ������ʣ����һ�����õ�ⷨ���ơ���ͭ���õ���ͭ�ĵĵ����У����������� ������������ ��������Ϊ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��16�֣�
��CaSO4����O2��ȼ��CO��Ӧ���ȿ������ȼ��Ч�ʣ����ܵõ��ߴ�CO2����һ�ָ�Ч����ࡢ���õ�����ȼ�ռ�������Ӧ��Ϊ����Ӧ����Ӧ�ں͢�Ϊ����Ӧ��
��1/4CaSO4(s)+CO(g)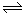 1/4CaS(s)+CO2(g) ��H1=��47.3kJ/mol
1/4CaS(s)+CO2(g) ��H1=��47.3kJ/mol
��CaSO4(s)+CO(g)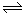 CaO(s)+ CO2(g)+ SO2(g) ��H2=+210.5kJ/mol
CaO(s)+ CO2(g)+ SO2(g) ��H2=+210.5kJ/mol
��CO(g)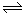 1/2C(s)+1/2CO2(g) ��H3=-86.2kJ/mol
1/2C(s)+1/2CO2(g) ��H3=-86.2kJ/mol
��1����Ӧ2 CaSO4(s)+7CO(g)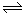 CaS(s)+CaO(s)+C(s)+6CO2(g)+SO2(g)�ġ�H= ���á�H1��H2��H3��ʾ����
CaS(s)+CaO(s)+C(s)+6CO2(g)+SO2(g)�ġ�H= ���á�H1��H2��H3��ʾ����
��2����Ӧ�١��۵�ƽ�ⳣ���Ķ���lgK�淴Ӧ�¶�T�ı仯����ͼ18.��ϸ���Ӧ�ġ�H������lgK��T���߱仯���ɣ�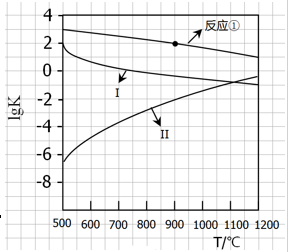
a��
b)
��3����ʢ��CaSO4����պ��������г���CO����Ӧ����900 ºC�ﵽƽ�⣬cƽ����CO��=8.0��10-5mol��L-1������CO��ת���ʣ����Ը���Ӧ���������2λ��Ч���֣���
��4��Ϊ���ٸ������ø�������CO2�����ڳ�ʼȼ������������ ��
��5���Է�Ӧ�������ɵ�CaSΪԭ�ϣ���һ�������¾�ԭ��������100%�ĸ��·�Ӧ����������CaSO4���÷�Ӧ�Ļ�ѧ����ʽΪ ����һ��������CO2����Զ��ױ���Ӧ�����䱽��������һ���Ȼ�������Ľṹ��ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
����P(s)��Cl2(g)������Ӧ����PCl3(g)��PCl5(g)����Ӧ���̺�������ϵ��ͼ��ʾ( ͼ�еġ�H��ʾ����1mol���������)������ͼʾ���ش��������⣺
��P��Cl2��Ӧ����PCl3(g)���Ȼ�ѧ����ʽ ��
��PCl5(g)�ֽ��PCl3(g)��Cl2���Ȼ�ѧ����ʽ ��
�ǰ�������ȼ�����ײ�����ȼ������ת��ɺ���Ϊ (���š�������) �ȷ�Ӧ������ð����������Cl2��Ӧ����1molPCl5�ġ�H3�����H3 ��H1 (������������� �� ������)��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com