
已知有如下反应:①2BrO3-+Cl2=Br2+2ClO3-,②2FeCl2+Cl2=2FeCl3,③2FeCl3+2KI═2FeCl2+2KCl+I2,④ClO3-+5Cl-+6H+═3Cl2+3H2O,下列各微粒氧化能力由强到弱的顺序正确的是
A.ClO3->BrO3->Cl2>Fe3+>I2
B.BrO3->Cl 2>ClO3->I2>Fe3+
C.BrO3->ClO3->Cl2>Fe3+>I2
D.BrO3->ClO3->Fe3+>Cl2>I2
科目:高中化学 来源:2015-2016学年海南省高二上12月段考化学试卷(解析版) 题型:填空题
煤气化和液化是现代能源工业中重点考虑的能量综合利用方案。最常见的气化方法为用煤生成水煤气,而当前比较流行的液化方法用煤生成CH3OH。
(1)已知:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H1
2CO(g)+O2(g)=2CO2(g) △H2
2H2(g)+O2(g)=2H2O(g) △H3
则反应CO(g) +2H2(g)=CH3OH(g) 的△H=_______。
(2)如图是该反应在不同温度下CO的转化率随时间变化的曲线。
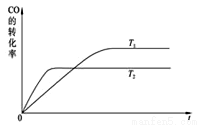
①T1和T2温度下平衡常数大小关系是K1____K2(填“>”“<”或“=”)。
②由CO合成甲醇时,CO在250℃、300℃、350℃下达到平衡时转化率与压强的关系曲线如下图所示,则曲线c所表示的温度为______℃,实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是______。

③以下有关该反应的说法正确的是_________(填序号)。
A.恒温、恒容条件下同,若容器内的压强不发生变化,则可逆反应达到平衡
B.一定条件下,H2的消耗速率是CO的消耗速率的2倍时,可逆反应达到平衡
C.使用合适的催化剂能缩短达到平衡的时间并提高CH3OH的产率
D.某温度下,将2molCO和6molH2充入2L密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为80%
(3)一定温度下,向2L固定体积的密闭容器中加入1molCH3OH,发生反应:CH3OH(g)  CO(g) +2H2(g),H2的物质的量随时间变化的曲线如图所示。
CO(g) +2H2(g),H2的物质的量随时间变化的曲线如图所示。

0~2min内的平均反应速率v(CH3OH)= ____________;该温度下,CO(g)+2H2(g) CH3OH(g)的平衡常数K=____________;相同温度下,若开始加入CH3OH(g)的物质的量是原来的2倍,则_____ 是原来的2倍.
CH3OH(g)的平衡常数K=____________;相同温度下,若开始加入CH3OH(g)的物质的量是原来的2倍,则_____ 是原来的2倍.
A.平衡常数 B.CH3OH的平衡浓度 C.达到平衡的时间 D.平衡时气体的密度
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二上第二次质检化学试卷(解析版) 题型:选择题
对于易燃、易爆、有毒的化学物质,往往会在其包装上贴上危险警告标签。下面所列物质中,标签贴错的是
A | B | C | D | |
物质的化学式 | 浓H2SO4 | 汽油 | 乙醇 | KNO3 |
危险警告标签 |
腐蚀品 |
易燃液体 |
剧毒品 |
爆炸品 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高一12月月考化学试卷(解析版) 题型:选择题
铁和氧化铁的混合物共amol,加盐酸后固体全部溶解,共收集到2bgH2,且溶液中加入KSCN溶液不显红色,则原混合物中铁的物质的量为
A.b mol B.(a-b)mol C.1/2(a?b)mol D.1/2(a+b)mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山西省高二上12月月考化学试卷(解析版) 题型:选择题
室温下,向下列溶液中通入相应的气体至溶液pH=7(通入气体对溶液体积的影响可忽略),溶液中部分微粒的物质的量浓度关系正确的是
A.向0.10mol•L-1NH4HCO3溶液中通入CO2:c(NH4+)=c(HCO3-)+c(CO32-)
B.向0.10mol•L-1NaHSO3溶液中通入NH3:c(Na+)>c(NH4+)>c(SO32-)
C.向0.10mol•L-1Na2SO3溶液通入SO2:c(Na+)=2[c(SO32-)+c]HSO3-)+c(H2SO3)]
D.向0.10mol•L-1CH3COONa溶液中通入HCl:c(Na+)>c(CH3COOH)=c(Cl-)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省高二上期中测试化学试卷(解析版) 题型:填空题
【加试题】节能减排已经成为全社会的共识,浙江省在原先推行乙醇汽油的基础上,开始试点甲醇汽油(即在汽油中添加一定量的甲醇),根据检测的数据分析认为,若绍兴全市的100余万辆机动车全部使用甲醇汽油,一年内能减少有害气体(一氧化碳)排放将近100万吨。甲醇常利用煤气化过程中生成的CO和H2来制备:CO+2H2?CH3OH 。
请根据图示回答下列:

(1)关于该自发反应的下列说法中,正确的是 (填字母):
A.△H>0,△S>0 B.△H>0,△S<0
C.△H<0,△S<0 D.△H<0,△S>0
(2)现进行如下实验,在体积为1L的密闭容器中,充入1molCO和3molH2,测得CO和CH3OH(g)的浓度随时间变化如图所示。从反应开始到平衡,CO的平均反应速率v(CO)= mol/(L•min),该反应的平衡常数K= 。
(3)恒容条件下,达到平衡后,下列措施中能使n(CH3OH)/n(CO)增大的有 。
A.升高温度 B.充入He气 C.再冲入1molCO和3molH2 D.使用催化剂
(4)若在一体积可变的密闭容器中充入1molCO、2molH2和1molCH3OH,达到平衡时测的混合气体的密度是同温同压下起始的1.6倍(此过程三种物质均处于气态),则平衡时混合气体的平均摩尔质量= g/mol。
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上12月月考化学试卷(解析版) 题型:实验题
盐卤中除含有Mg2+、Cl-外,还含有少量Na+、Fe2+、Fe3+、SO42-和CO(NH2)2等。从海水提取食盐和Br2后的盐卤中可以提取MgCl2、MgO、Mg(OH)2等物质,制备流程如图所示:
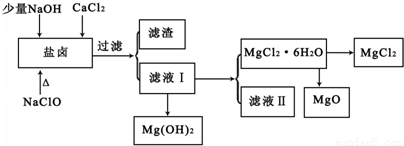
(1)从MgCl2溶液得到MgCl2.6H2O晶体的过程中所需的基本操作顺序依次为_________________ ;
A.加热蒸馏B.加热浓缩C.冷却结晶D.趁热过滤 E.过滤洗涤
(2)制取无水氯化镁必须在氯化氢存在的条件下进行,原因是____________(用适当的文字结合化学用语说明)。
(3)用NaClO除去尿素CO(NH2)2时,生成物除盐外,都是能参与大气循环的物质,则该反应的化学方程式为_________________ ;加入NaClO的另一个作用是_________________。
(4)Mg(OH)2是制镁盐、耐火材料和阻燃剂的重要原料.
已知25℃时Ksp[Mg(OH)2]=5.6×10-12,且Mg(OH)2(s)═MgO(s)+H2O(s)△H=+81.5kJ/mol.
①下列叙述正确的是_________
A.从盐卤或海水中获得Mg(OH)2,工业上选择NaOH作沉淀剂
B.Mg(OH)2能作阻燃剂的原因是它分解吸热且生成MgO覆盖可燃物
C.可加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁
②酸碱指示剂百里酚蓝变色的pH范围如下:
pH | <8.0 | 8.0~9.6 | >9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25℃时,在Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液的颜色为______。
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期第四次调研化学试卷(解析版) 题型:选择题
下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是
选项 | 叙述Ⅰ | 叙述Ⅱ |
A | Fe3+具有氧化性 | Fe2(SO4)3可作净水剂 |
B | 浓硫酸有腐蚀性 | 常温下浓硫酸不能用铁罐盛装 |
C | 将鸡蛋壳置于醋酸中浸泡一段时间鸡蛋壳大部分溶解且有气泡冒出 | 醋酸的酸性强于碳酸 |
D | 向漂白粉中滴加少量浓盐酸产生刺激性气味气体 | 漂白粉已经变质 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东汕头金山中学高一上12月月考化学卷(解析版) 题型:选择题
关于钠在空气中燃烧的实验,下列说法不正确的是
A.用镊子夹取钠块,吸干表面的煤油后,用小刀切下一部分进行实验。剩余的钠应放回原试剂瓶。
B.钠加热后先熔化成小球状,这是因为金属钠的熔点较低。
C.钠燃烧时火焰呈黄色,这与钠元素的焰色反应有关。
D.钠块表面若有部分已被氧化为Na2O,充分燃烧后将得到Na2O和Na2O2的混合物。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com