
| A、1mol/L硫酸溶液所含的H+数约为1.204×1024个 |
| B、标准状况下气体摩尔体积约为22.4L |
| C、0.5 L 1 mol/L FeCl3溶液与0.2 L 1 mol/L KCl溶液中的Cl-的数目之比为15:2 |
| D、100 mL 1 mol/L NaCl溶液与50 mL 1 mol/L AlCl3溶液中Cl-物质的量浓度相等 |


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
| A、若B是气体,增大A的浓度会使B转化率增大 |
| B、若增大A的浓度,平衡体系颜色加深,D不一定是有颜色的气体 |
| C、升高温度,C百分含量减少,说明正反应是放热反应 |
| D、增大压强,平衡不移动,说明B、D是气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢气和氯气反应生成氯化氢气体的热化学方程式是 H2(g)+Cl2(g)=2HCl(g) |
| B、氢气和氯气反应生成 2mol 氯化氢气体,反应的△H=183kJ/mol |
| C、氢气和氯气反应生成 2mol 氯化氢气体,反应的△H=-183kJ/mol |
| D、氢气和氯气反应生成 1mol 氯化氢气体,反应的△H=-183kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含NaOH 0.1mol |
| B、c(Na+)为1mol/L |
| C、含NaOH 4g |
| D、c(OH-)为0.1mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、从1 L 1 mol/L的NaCl溶液中取出100 mL,其浓度为0.1 mol/L |
| B、配制0.5 L 10 mol/L的盐酸,需要氯化氢气体112 L |
| C、0.5 L 2 mol/L BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 |
| D、10 g 98%的硫酸(密度为1.84 g/cm3)与10 mL 18.4 mol/L硫酸的浓度是不同的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K在空气中可以被空气中的氧气氧化 |
| B、K可以与乙醇发生反应生成氢气 |
| C、K与水的反应不如钠与水的反应剧烈 |
| D、K也可放在煤油中保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验 编号 | a中试剂 | b中试剂 | 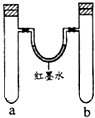 |
| 1 | 0.1克Na、3mL水 | 0.1克Na、3mL乙醇 | |
| 2 | 3mL水 | 3mL饱和FeSO4溶液 | |
| 3 | 3mL浓硝酸、1g铝片 | 3mL浓硝酸、1g铜片 | |
| 4 | 生铁钉、3mL饱和食盐水 | 生铁钉、3mL饱和氯化铵 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com