
”¾ĢāÄæ”æÓĆ“æ¾»µÄCaCO3Óė100mLĻ”ŃĪĖį·“Ó¦ÖĘČ”CO2£¬ŹµŃé¹ż³Ģ¼ĒĀ¼ČēĶ¼ĖłŹ¾£ØCO2µÄĢå»żŅŃÕŪĖćĪŖ±ź×¼×“æöĻĀµÄĢå»ż£©”£

¢ÅĻĀĮŠ·ÖĪö²»ÕżČ·µÄŹĒ________”£
A£®OE¶Ī±ķŹ¾µÄĘ½¾łĖŁĀŹ×īæģ
B£®EF¶Ī£¬ÓĆŃĪĖį±ķŹ¾øĆ·“Ó¦µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.4mol/£ØL”¤min£©
C£®EF¶Ī±ķŹ¾µÄĘ½¾łĖŁĀŹ×īæģ,Ö÷ŅŖŌŅņŹĒ·“Ó¦·ÅČČ
D£®Gµć±ķŹ¾ŹÕ¼ÆµÄCO2µÄĮæ×ī¶ą
¢ĘĪŖĮĖ½µµĶÉĻŹö»Æѧ·“Ó¦µÄ·“Ó¦ĖŁĀŹ£¬ÓūĻņČÜŅŗÖŠ¼ÓČėĻĀĮŠĪļÖŹ£¬ÄćČĻĪŖæÉŠŠµÄŹĒ______”£
A£®ÕōĮóĖ® B£®NaCl¹ĢĢå C£®CH3COONa¹ĢĢå D£®ÅØŃĪĖį
¢Ē³żĮĖÉĻŹö·½·ØĶā£¬ÄćČĻĪŖ»¹æÉŅŌ²ÉČ”ÄÄŠ©“ėŹ©Ą“½µµĶ»Æѧ·“Ó¦ĖŁĀŹ?
__________________________________________________(ĢīŅ»ÖÖ·½·Ø¼“æÉ)”£
”¾“š°ø”æ A AC ½µµĶ·“Ó¦ĪĀ¶Č£ØĘäĖüŗĻĄķ“š°ø¾łµĆ·Ö£©
”¾½āĪö”æ£Ø1£©A£®Š±ĀŹ±ķŹ¾·“Ó¦ĖŁĀŹ£¬Š±ĀŹŌ½“ó·“Ó¦ĖŁĀŹŌ½“ó£¬ÓÉĶ¼æÉÖŖ£¬EF¶ĪŠ±ĀŹ×ī“ó£¬ĖłŅŌEF¶Ī·“Ó¦ĖŁĀŹ×ī“ó£¬A“ķĪó£»B£®ÓÉĶ¼æÉÖŖEF¶ĪÉś³ÉµÄ¶žŃõ»ÆĢ¼µÄĢå»żĪŖ672mL£224mL=448mL£¬ĖłŅŌ¶žŃõ»ÆĢ¼µÄĪļÖŹµÄĮæĪŖ0.448L”Ā22.4L/mol=0.02mol£¬øł¾ŻCaCO3+2HCl£½CaCl2+CO2”ü+H2O£¬æÉÖŖ²Ī¼Ó·“Ó¦µÄĀČ»ÆĒāµÄĪļÖŹµÄĮæĪŖ0.04mol£¬ĖłŅŌŃĪĖįµÄÅØ¶Č±ä»ÆĮæĪŖ0.04mol”Ā0.1L=0.4mol/L£¬ĖłŅŌEF¶ĪÓĆŃĪĖį±ķŹ¾øĆ·“Ó¦µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ0.4mol/L”Ā1min
=0.4mol/£ØLmin£©£¬BÕżČ·£»C£®EF¶ĪÅضČÖš½„¼õŠ”£¬µ«ĪĀ¶ČÉżøߣ¬µ¼ÖĀ·“Ó¦ĖŁĀŹŌö“ó£¬CÕżČ·£»D£®Gµć±ķŹ¾ŹÕ¼ÆµÄ¶žŃõ»ÆĢ¼ĪŖ“ÓæŖŹ¼µ½GµćÉś³ÉµÄ¶žŃõ»ÆĢ¼£¬×ܹ²784mL£¬DÕżČ·£¬“š°øŃ”A”££Ø2£©A£®¼ÓČėÕōĮóĖ®£¬ČÜŅŗÅØ¶Č½µµĶ£¬·“Ó¦ĖŁĀŹ¼õŠ”£¬AÕżČ·£»B£®NaCl¹ĢĢ壬ČÜŅŗÅØ¶Č²»±ä£¬·“Ó¦ĖŁĀŹ²»±ä£¬B“ķĪó£»C£®¼ÓČėCH3COONa¹ĢĢ壬ĒāĄė×ÓÅØ¶Č¼õŠ”£¬·“Ó¦ĖŁĀŹ¼õŠ”£¬CÕżČ·£»D£®¼ÓČėÅØŃĪĖį£¬ĒāĄė×ÓÅضČŌö“󣬷“Ó¦ĖŁĀŹŌö“ó£¬D“ķĪ󣬓š°øŃ”AC£»£Ø3£©³ż½µµĶ·“Ó¦ÅضČÖ®Ķā£¬½µµĶ·“Ó¦ĪĀ¶ČµČ£¬Ņ²æɼõŠ”·“Ó¦ĖŁĀŹ”£


 ĆææĪ±ŲĮ·ĻµĮŠ“š°ø
ĆææĪ±ŲĮ·ĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ(1)ŅŃÖŖH£«(aq)£«OH£(aq)===H2O(l) ¦¤H£½£57.3 kJmol-1”£ČōĻņČż·ŻµČĢå»ż”¢µČĪļÖŹµÄĮæÅØ¶ČµÄNaOHČÜŅŗÖŠ·Ö±š¼ÓČė“×Ėį”¢ÅØĮņĖį”¢Ļ”ĻõĖįÖĮĒ”ŗĆĶźČ«·“Ó¦£¬²¢½«ÉĻŹö¹ż³ĢÖŠ·Å³öµÄČČĮæ·Ö±š¼ĒĪŖQ1kJ”¢Q2kJ”¢Q3kJ”£ŌņČżÕßµÄÓÉŠ”µ½“ó¹ŲĻµŹĒ________(ÓĆQ1”¢Q2”¢Q3±ķŹ¾)”£
(2)ČēĶ¼ĖłŹ¾AĪŖÅŻÄĖÜĮĻ°å£¬ÉĻĆęÓŠĮ½øöŠ”æ×£¬·Ö±š²åČėĪĀ¶Č¼ĘŗĶ»·ŠĪ²£Į§½Į°č°ō£¬Į½øöŠ”æײ»ÄÜæŖµĆ¹ż“ó£¬ĘäÄæµÄŹĒ_____________________£» ČōŹµŃéÖŠ²»¼ÓøĒÅŻÄĖÜĮĻ°å£¬ŌņĒóµĆµÄÖŠŗĶČČŹżÖµ______£ØĢīĘ«“ó”¢Ę«Š””¢ĪŽÓ°Ļģ£©

(3)ŹµŃéŹŅÓĆ50mL 0.50molL-1ŃĪĖį”¢50mL 0.55molL-1 NaOHČÜŅŗĄūÓĆÉĻĶ¼×°ÖĆ£¬½ųŠŠ²ā¶ØÖŠŗĶČȵďµŃ锣¼ŁÉčŃĪĖįŗĶĒāŃõ»ÆÄĘČÜŅŗµÄĆܶȶ¼ŹĒ1 g/cm3£¬ÓÖÖŖÖŠŗĶŗóÉś³ÉČÜŅŗµÄ±ČČČČŻc£½4.18 J/(g”ę)”£ĪŖĮĖ¼ĘĖćÖŠŗĶČČ£¬ŹµŃ鏱»¹Šč²āĮæµÄŹż¾ŻÓŠ(ĢīŠņŗÅ)________”£
A£®·“Ó¦Ē°ŃĪĖįµÄĪĀ¶Č B£®·“Ó¦Ē°ŃĪĖįµÄÖŹĮæ
C£®·“Ó¦Ē°ĒāŃõ»ÆÄĘČÜŅŗµÄĪĀ¶Č D£®·“Ó¦Ē°ĒāŃõ»ÆÄĘČÜŅŗµÄÖŹĮæ
E£®·“Ó¦ŗó»ģŗĻČÜŅŗµÄ×īøßĪĀ¶Č F£®·“Ó¦ŗó»ģŗĻČÜŅŗµÄÖŹĮæ
(4)Ä³Ń§ÉśŹµŃé¼ĒĀ¼Źż¾ŻČēĻĀ£ŗ
ŹµŃéŠņŗÅ | ĘšŹ¼ĪĀ¶Čt1/”ę | ÖÕÖ¹ĪĀ¶Čt2/”ę | |
ŃĪĖį | ĒāŃõ»ÆÄĘČÜŅŗ | »ģŗĻČÜŅŗ | |
1 | 20.0 | 20.1 | 23.4 |
2 | 20.2 | 20.4 | 23.6 |
3 | 20.5 | 20.6 | 23.8 |
ŅĄ¾ŻøĆѧɜµÄŹµŃ鏿¾Ż¼ĘĖć£¬øĆŹµŃé²āµĆµÄÖŠŗĶČȦ¤HĪŖ________”£(±£ĮōČżĪ»ÓŠŠ§Źż×Ö)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷×éÖŠµÄĮ½ĪļÖŹĻą»„·“Ó¦Ź±£¬Čōøı䷓ӦĢõ¼ž(ĪĀ¶Č”¢·“Ó¦ĪļÓĆĮæ±Č)£¬»Æѧ·“Ó¦µÄ²śĪļ²¢²»øıäµÄŹĒ( )
A. NaŗĶO2 B. NaOHŗĶCO2 C. Na2O2ŗĶCO2 D. ľĢæ(C)ŗĶO2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
A. ĀóŃæĢĒŗĶÕįĢĒµÄĖ®½ā²śĪļĻąĶ¬B. ĢģČ»ÓĶÖ¬ŹōÓŚõ„ĄąĪļÖŹ
C. µķ·ŪŗĶĻĖĪ¬ĖŲµÄ·Ö×ÓŹ½²»Ķ¬D. ŹÆÓĶĮŃ»ÆŗĶĮŃ½ā¶¼æÉÖʵĆĻ©Ģž
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅ»¶ØĪĀ¶ČĻĀ£¬·“Ó¦2SO2+O2![]() 2SO3£¬“ļµ½Ę½ŗāŹ±£¬n(SO2)£ŗn(O2)£ŗn(SO3)=2£ŗ3£ŗ4”£ĖõŠ”Ģå»ż£¬·“Ó¦ŌŁ“Ī“ļµ½Ę½ŗāŹ±£¬n(O2)=0.8 mol£¬n(SO3)=1.4 mol£¬“ĖŹ±SO2µÄĪļµÄĮæÓ¦ŹĒ£Ø £©
2SO3£¬“ļµ½Ę½ŗāŹ±£¬n(SO2)£ŗn(O2)£ŗn(SO3)=2£ŗ3£ŗ4”£ĖõŠ”Ģå»ż£¬·“Ó¦ŌŁ“Ī“ļµ½Ę½ŗāŹ±£¬n(O2)=0.8 mol£¬n(SO3)=1.4 mol£¬“ĖŹ±SO2µÄĪļµÄĮæÓ¦ŹĒ£Ø £©
A. 0.4 mol B. 0.6 mol C. 0.8 mol D. 1.2 mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·ØÖŠ£¬ÕżČ·µÄŹĒ( )
A. ·ÖŅŗĀ©¶·æÉÓĆÓŚ·ÖĄė±½ŗĶĖ®£¬ĒŅ±½²ćÓÉ·ÖŅŗĀ©¶·µÄĻĀæŚĮ÷³ö
B. ĄūÓƶ”“ļ¶ūŠ§Ó¦æÉŅŌĒų·ÖČÜŅŗÓė½ŗĢå
C. ÓĆijČÜŅŗ×öŃęÉ«·“Ó¦ŹµŃ鏱»šŃęĪŖ»ĘÉ«£¬ŌņøĆČÜŅŗÖŠŅ»¶ØÓŠÄĘŌŖĖŲ£¬Ć»ÓŠ¼ŲŌŖĖŲ
D. ÅäÖĘĮņĖįČÜŅŗŹ±£¬æÉĻČŌŚČŻĮæĘæÖŠ¼ÓČėŅ»¶ØĢå»żµÄÅØĮņĖį£¬ŌŁŌŚ½Į°čĻĀĀżĀż¼ÓČėĖ®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗćĪĀĻĀ£¬½«2molSO2ŗĶ1mo O2µÄ»ģŗĻĘųĢåĶØČėŅ»øöČŻ»ż¹Ģ¶ØµÄ5LĆܱÕČŻĘ÷ÖŠ£¬·¢ÉśČēĻĀ·“Ó¦£ŗ2SO2£Øg£©+O2 (g) ![]() 2SO3 (g)
2SO3 (g)
£Ø1£©Čō2·ÖÖÓŗ󣬲āµĆO2µÄÅضČĪŖ0.1mol/L£¬Ōņ2·ÖÖÓÄŚO2µÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖ____________”£
£Ø2£©5·ÖÖÓŗó·“Ó¦“ļĘ½ŗā£¬»ģŗĻĘųĢåµÄĪļÖŹµÄĮæĪŖ2.4mol£¬ŌņĘ½ŗāŹ±SO3µÄĪļÖŹµÄĮæĪŖ_______________ ”£
£Ø3£©“ļĘ½ŗāŹ±£¬SO2µÄ×Ŗ»ÆĀŹĪŖ____________ £¬Ę½ŗāŹ±ČŻĘ÷ÄŚµÄŃ¹ĒæÓėĘšŹ¼Ź±µÄŃ¹ĒæÖ®±ČĪŖ___________ ”£
£Ø4£©ČōĘ½ŗāŗó£¬ĻņøĆČŻĘ÷ÖŠ³äČėŅ»¶ØĮæµÄė²Ęų£¬»ÆŃ§Ę½ŗā½«_____________ ”££ØÕżĻņŅĘ¶Æ”¢ÄęĻņŅĘ¶Æ”¢²»ŅĘ¶Æ£©£»ČōĘ½ŗāŗó£¬ĻņøĆČŻĘ÷ÖŠŌŁ³äČė2molSO2ŗĶ1molO2£¬µ±·“Ó¦ŌŁ“Ī“ļĘ½ŗāŹ±£¬SO2µÄ×Ŗ»ÆĀŹ½«____________ £ØŌö“󔢼õŠ””¢²»±ä£©”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻÖÓŠČēĻĀĮ½øö·“Ó¦£ŗ(A)NaOH£«HCl===NaCl£«H2O””(B)2FeCl3£«Cu===2FeCl2£«CuCl2
(1)øł¾ŻĮ½·“Ó¦±¾ÖŹ£¬ÅŠ¶ĻÄÜ·ńÉč¼Ę³ÉŌµē³Ų(Ģī”°ÄÜ”±»ņ”°²»ÄÜ”±)(A)______£¬(B)________£»
(2)Čē¹ū(A»ņB)²»ÄÜ£¬ĖµĆ÷ĘäŌŅņ_________________________________________£»
(3)Čē¹ū(A»ņB)æÉŅŌ£¬ŌņŌŚĻĀĆę·½æņÖŠ»³ö×°ÖĆĶ¼²¢Š“³öÕż”¢øŗ¼«²ÄĮĻ¼°µē¼«·“Ó¦Ź½
________
øŗ¼«£ŗ________”¢_______________________________________£»
Õż¼«£ŗ________”¢________________________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĶ¼ĪŖŌŖĖŲÖÜĘŚ±ķÖŠĒ° 4 ÖÜĘŚµÄ±ķøń”£
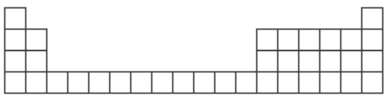
¼×ŹĒŅ»ÖÖ³£¼ū»ÆŗĻĪļ£¬Ęä»ÆѧŹ½ĪŖ XC13”£
£Ø1£©øł¾ŻÄćĖłŃ§ÖŖŹ¶£¬½« X “ś±ķµÄŌŖĖŲ·ūŗÅ£¬ĢīŌŚĖłøųÖÜĘŚ±ķµÄ±ķøńÖŠ¶ŌÓ¦µÄĪ»ÖĆ__________£ØÖ»Š“³ö2 ÖÖ¼“æÉ£©
£Ø2£©Čō½«Ņ»ÖÖXC13Ė®ČÜŅŗÕōøÉ”¢×ĘÉÕ£¬µĆµ½ŗģ×ŲÉ«·ŪÄ© X2O3£¬Ōņŗ¬Ģ¼µÄ X ŗĻ½šŌŚ³±ŹŖµÄ£ØÖŠŠŌ»·¾³£©æÕĘųÖŠ·¢Éśµē»ÆøÆŹ“Ź±µÄÕż¼«·“Ó¦Ź½ĪŖ__________”£
£Ø3£©Čō X“ś±ķĮķŅ»ÖÖ½šŹōµ„ÖŹ£¬øƵ„ÖŹæÉÓė£Ø2£©ÖŠĖłŹöµÄ·ŪÄ©·¢Éś·“Ó¦£¬øĆ·“Ó¦æÉÓĆÓŚ_____”££ØŠ“³öŅ»ÖÖÓĆĶ¾£©£»øĆŌŖĖŲµÄĮņĖįŃĪ£ØŌ¼1 mol”¤L£1£©ŗĶNaHCO3ČÜŅŗ£ØŌ¼1 mol”¤L£1£©¼°ĘšÅŻ¼ĮÖĘ³ÉÅŻÄĆš»š¼Į”£Ź¹ÓĆŹ±·¢ÉśµÄ»Æѧ·“Ó¦·½³ĢŹ½ŹĒ_______________________________£¬¶žÕßµÄĢå»ż±ČŌ¼ŹĒ________”£ÅŻÄĆš»šĘ÷ÄŚµÄ²£Į§Ķ²ĄļŹ¢ X ŌŖĖŲµÄĮņĖįŃĪČÜŅŗ£¬ĪŖŹ²Ć“²»ÄÜ°ŃĖüŹ¢·ÅŌŚĢśĶ²Ąļ________£ØÓĆĄė×Ó·½³ĢŹ½½āŹĶ£©
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com