
为测某镁铝合金样品中铝的含量,进行下列实验:取一定量合金,加入100mL0.3mol·L—1稀硫酸,合金完全溶解,产生的气体在标准状况下体积为560mL;再加0.2mol·L—1NaOH溶液至沉淀质量恰好在此时不再变化,用去350mL NaOH溶液。则所取样品中铝的物质的量为
A.0.005mol B.0.01mol C.0.025mol D.0.03mol
B
【解析】
试题分析:根据题意,稀硫酸为0.03mol,氢气为0.025mol,氢氧化钠用去0.07mol,加入氢氧化钠反应如下:
首先发生的反应是中和过量的酸:H++OH-=H2O,
然后是沉淀两种金属离子:Mg2++2OH-=Mg(OH)2↓、Al3++3OH-=Al(OH)3↓,
最后是Al(OH)3的溶解:Al(OH)3+OH-=[Al(OH)4]-
沉淀的量不再变化,说明Na+最终生成的是Na2SO4为0.03mol,则NaAlO2为0.01mol,Al为0.01mol。
考点:考查镁铝的性质及化学计算。
点评:对于金属参与反应化学计算,一般可采用守恒法计算。


科目:高中化学 来源: 题型:阅读理解
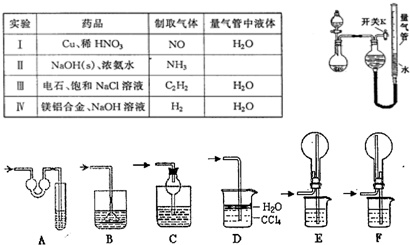
| 编号 | 镁铝合金度量 | 量气管第一次读数 | 量气管第二次读数 |
| ① | 1.0g | 10.0mL | 346.3mL |
| ② | 1.0g | 10.0mL | 335.0mL |
| ③ | 1.0g | 10.0mL | 345.7mL |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 18a |
| 22.4w |
| 18a |
| 22.4w |
查看答案和解析>>
科目:高中化学 来源:2011-2012学年吉林省长春外国语学校高一上学期期末考试理科化学试卷 题型:实验题
某同学设计了一个简单的实验(如图所示),以测定镁铝合金中铝的质量分数。可供选用的试剂有:浓H2SO4、浓硝酸、6 mol·l-1 NaOH溶液。
请填写下列空白
(1)有关实验操作:a、往试管中放入适量的铝合金样品;b、从分液漏斗往试管中加入过量的A溶液;c、检查装置的气密性;d、测定收集到的水的体积。正确的操作顺序是
(2)A中可选用的溶液是
(3)实验中发生反应的化学方程式为
(4)若实验中测得样品的质量为W g ,氢气的体积为aL (标准状况),则样品中Al的质量分数为
查看答案和解析>>
科目:高中化学 来源:2014届广东省高一11月月考化学试卷 题型:实验题
(7分)某同学设计了一个简单的实验(如图所示),以测定镁铝合金中铝的质量分数。可供选用的试剂有:浓H2SO4、浓硝酸、6 mol·L-1 NaOH溶液。

请填写下列空白:
(1)有关实验操作:a、往试管中放入适量的铝合金样品;b、从分液漏斗往试管中加入过量的A溶液;c、检查装置的气密性;d、测定收集到的水的体积。
正确的操作顺序为_______________________________(填字母)。
(2)A溶液可选用___________________________________________
(3)写出实验中发生反应的化学方程式:_________________________________________。
(4)若实验中测得样品的质量为Wg ,氢气的体积为a L(标准状况),则样品中Al的质量分数为_ __。
查看答案和解析>>
科目:高中化学 来源:2014届吉林省高一上学期期末考试理科化学试卷 题型:实验题
某同学设计了一个简单的实验(如图所示),以测定镁铝合金中铝的质量分数。可供选用的试剂有:浓H2SO4、浓硝酸、6 mol·l-1 NaOH溶液。

请填写下列空白
(1)有关实验操作:a、往试管中放入适量的铝合金样品;b、从分液漏斗往试管中加入过量的A溶液;c、检查装置的气密性;d、测定收集到的水的体积。正确的操作顺序是
(2)A中可选用的溶液是
(3)实验中发生反应的化学方程式为
(4)若实验中测得样品的质量为W g ,氢气的体积为aL (标准状况),则样品中Al的质量分数为
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com