
某链烃3.6g和Cl2发生取代反应,控制反应条件使其仅生成一氯代物,将反应生成的气体(一氯代物为液体)用NaOH溶液吸收恰好和0.1mol·L-1 NaOH溶液500mL完全反应,试解答下列问题:(1)求该烃的相对分子质量;(2)若该烃既不能使酸性KMnO4溶液褪色,又不能使溴水褪色,试求该烃的分子式。(3)若该烃的一氯代物只有一种,试确定该烃的结构简式 (要求写出计算过程)
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列操作能达到实验目的的是 ( )
| 目 的 | 操 作 | |
| A | 确定某卤代烃为氯代烃 | 取某卤代烃少许与NaOH溶液共热后再加盐酸酸化,然后加AgNO3溶液,有白色沉淀 |
| B | 配制银氨溶液 | 在硝酸银溶液中滴加氨水至沉淀恰好消失 |
| C | 提取碘水中的碘 | 将碘水倒入分液漏斗,加入适量乙醇,振荡后静置 |
| D | 确定蔗糖是否发生水解 | 取2 mL水解液滴加少量新制的Cu(OH)2悬浊液,加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是
①离子化合物一定含离子键,也可能含极性键或非极性键
②同位素的性质几乎完全相同
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤由分子组成的物质中一定存在共价键
A.①③⑤ B.②④ C.①③ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)Zn粒和稀盐酸反应一段时间后,反应速率会减慢,当加热或加入浓盐酸后,反应速率明显加快。由此判断,影响化学反应速率的因素有 和 。
(2)为探究锌与盐酸反应过程的速率变化,某同学的实验测定方法是:在100ml稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如下(氢气体积已换算为标准状况):
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 体积/mL | 50 | 120 | 232 | 290 | 310 |
①哪一时间段反应速率最大_______(填“0~1 min”或“1~2 min”或“2~3 min”或“3~4 min”或“4~5min”)。
②2~3 min时间段以盐酸的浓度变化来表示的该反应速率(设溶液体积不变)为________。
③试分析1~3min时间段里,反应速率变大的主要原因 。
(3)对于容积固定的反应:N2(g)+3H2(g) 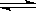 2NH3(g)(正反应放热),达到平衡的标志有___ 。
2NH3(g)(正反应放热),达到平衡的标志有___ 。
A.N2、H2、NH3的百分含量不再变化 B.总压强不变
C.N2、H2、NH3的分子数之比为1∶3∶2 D.N2、H2、NH3的浓度相等
E.N2、H2不再起反应 F.v(N2)=v(H2)
G.混合气体的密度不变 H.混合气体的平均相对分子质量不变
I.正反应放出的热量等于逆反应吸收的热量
查看答案和解析>>
科目:高中化学 来源: 题型:
从海带中提取碘的实验过程中,涉及到下列操作,其中正确的是(考察每一个操作时,假设其它操作均正确)( )
|
|
|
|
|
A.将海带灼烧成灰 B.过滤得合I—溶液 C.放出碘的苯溶液 D.分离碘并回收苯
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中微粒浓度关系一定正确的是( )
A.常温下,氨水与氯化铵的pH=7的混合溶液中:c(Cl-)>c(NH4+)
B.常温下,pH=2的一元酸和pH=12的一元强碱等体积混合: c(OH-)=c(H+)
C.0.1 mol·L—1的硫酸铵溶液中:c(NH4+)>c(SO42-)>c(H+)
D.0.1 mol·L—1的硫化钠溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S)
查看答案和解析>>
科目:高中化学 来源: 题型:
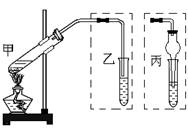 如图在甲处的试管中先加入2mL 95%的乙醇, 并在摇动下缓缓加入5mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在乙处的试管中加入5mL
如图在甲处的试管中先加入2mL 95%的乙醇, 并在摇动下缓缓加入5mL浓硫酸,充分摇匀,冷却后再加入2g无水乙酸钠,用玻璃棒充分搅拌后将试管固定在铁架台上,在乙处的试管中加入5mL
饱和碳酸钠溶液,按图连接好装置,用酒
精灯对甲处的试管缓慢加热,当观察到乙
处的试管中有明显现象时停止实验。请回答:
(1)甲处的试管内发生最主要反应的化学方程式为:
。
(2)题干中的“明显现象”指的是: 。
(3)在本实验中,加入浓硫酸的作用是 : 。
(4)该实验中长导管的作用是: 。
(5)饱和Na2CO3溶液的作用是:
。
(6)有人提议,最好把乙装置换成丙装置(小试管内仍为饱和Na2CO3溶液),原因有二: 一是可有效防止未被冷却的蒸气漂散到空气中,二是
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com