
| A. | 大于C | B. | 小于C | C. | 等于C | D. | 不能确定 |
分析 质量分数为2P,密度为d(d>1g/cm3),物质的量浓度为2C的浓硫酸中有:2C=$\frac{1000d•2p}{98}$;设稀释后溶液的密度为ρ,则稀释后的物质的量浓度C1=$\frac{1000ρp}{98}$,根据浓硫酸稀释后密度变小来分析.
解答 解:质量分数为2P,密度为d(d>1g/cm3),物质的量浓度为2C的浓硫酸中有:2C=$\frac{1000d•2p}{98}$,即C=$\frac{1000dp}{98}$;
设稀释后溶液的密度为ρ,则稀释后的物质的量浓度C1=$\frac{1000ρp}{98}$,由于浓硫酸稀释后密度变小,则有:C1=$\frac{1000ρp}{98}$<$\frac{1000dp}{98}$=c,故有稀释后的物质的量浓度C1<C,故选B.
点评 本题考查了浓硫酸稀释后的有关计算,难度不大,应注意的是浓硫酸稀释后浓度、密度和质量分数均变小.


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:解答题
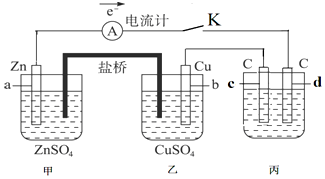
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
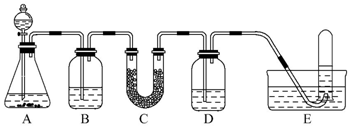
| 仪器 | 加入试剂 | 加入该试剂的目的 |
| B | 饱和NaHCO3溶液 | 除去CO2中混有的HCl |
| C | ||
| D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镀锡的铁皮,破损后铁皮反而易被腐蚀 | |
| B. | 纯铁比生铁更易被腐蚀 | |
| C. | 金属的电化腐蚀比化学腐蚀普遍 | |
| D. | 金属腐蚀的本质是M-ne-=Mn+而被损耗 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

 的系统命名4-甲基-2-乙基-1-戊烯
的系统命名4-甲基-2-乙基-1-戊烯 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe(OH)3溶于HI溶液中:Fe(OH)3+3H+═Fe3++3H2O | |
| B. | 磁性氧化铁溶于稀盐酸:Fe3O4+8H+═Fe3++2Fe2++4H2O | |
| C. | NaAlO2溶液中通入过量CO2:AlO2-+CO2+2H2O═Al(OH)3↓+HCO3- | |
| D. | 酸性高锰酸钾溶液和硫酸亚铁溶液反应:MnO4-+3Fe2++4H+═MnO2↓+3Fe3++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若A2和B2的总能量之和大于生成的AB的总能量,则反应吸热 | |
| B. | 若A2和B2的总能量之和小于生成的AB的总能量,则反应放热 | |
| C. | 若该反应为放热反应,则Q1+Q2<2Q3 | |
| D. | 若该反应为吸热反应,则Q1+Q2<Q3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com