
| A. | W可能是非金属元素 | |
| B. | X可能是氧化物 | |
| C. | Y、Z之间的转化可能是氧化还原反应 | |
| D. | Y和Z在溶液中反应可能生成X |
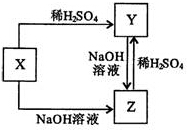
分析 由转化关系可知X既能与酸反应,也能与碱反应后,如X为单质,应为Al,如为化合物,可能为Al2O3、Al(OH)3、弱酸的酸式盐或弱酸弱碱盐等,以此解答该题.
解答 解:由转化关系可知X既能与酸反应,也能与碱反应后,如X为单质,应为Al,如为化合物,可能为Al2O3、Al(OH)3、弱酸的酸式盐或弱酸弱碱盐等,
A.如X为NaHCO3,则Y为CO2,Z为Na2CO3,都含有C元素,为非金属元素,故A正确;
B.如X为Al2O3,则Y为Al2(SO4)3、Z为NaAlO2,故B正确;
C.Y、Z可为NaHCO3、Na2CO3;Al2(SO4)3、NaAlO2等,之间可通过复分解反应实现,不是氧化还原反应,故C错误;
D.如X为Al(OH)3,Y为Al2(SO4)3、Z为NaAlO2,Al2(SO4)3、NaAlO2可发生互促水解反应生成Al(OH)3,故D正确.
故选C.
点评 本题考查无机物的推断,为高频考点和常见题型,侧重于元素化合物知识的综合理解和运用的考查,解答本题,注意把握两性物质的种类和性质,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 可以利用电泳现象区分溶液和胶体 | |
| B. | 可以利用胶体的丁达尔效应区分溶液和胶体 | |
| C. | 可以用过滤的方法分离溶液和胶体 | |
| D. | 溶液呈电中性,胶体是带电的 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 $→_{△}^{-H_{20}}$CH3CH=CHCHO,水杨酸酯E为紫外线吸收剂,可用于配制防晒霜.E的一种合成路线如下:
$→_{△}^{-H_{20}}$CH3CH=CHCHO,水杨酸酯E为紫外线吸收剂,可用于配制防晒霜.E的一种合成路线如下:
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 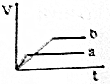 | B. | 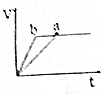 | C. |  | D. | 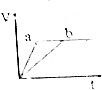 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
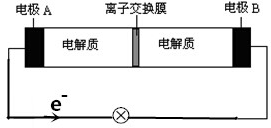
| A. | 放电时,Na+从右到左通过离子交换膜 | |
| B. | 放电时,负极反应式为3NaBr-2e-═NaBr3+2Na+ | |
| C. | 充电时,A极应与直流电源负极相连 | |
| D. | 放电时,当有0.1molNa+通过离子交换膜时,B极上有0.3molNaBr产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加热 | B. | 使用催化剂 | C. | 加压 | D. | 分离出D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2CO3 比NaHCO3 的溶解度大 | |
| B. | Na2CO3 比NaHCO3 稳定 | |
| C. | 物质的量相等的Na2CO3 和NaHCO3,前者质量大 | |
| D. | 物质的量相等的Na2CO3 和NaHCO3分别与足量盐酸反应得CO2 的物质的量之比为2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com