
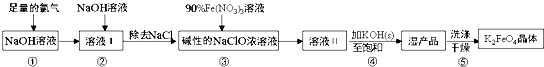
| A�� | ��������������뻹ԭ�������ʵ���֮��Ϊ3��2 | |
| B�� | �������Na2FeO4ת��Ϊʪ��Ʒ����ΪK2FeO4�ܽ�ȸ�С | |
| C�� | ������е�ϴ�Ӽ�����CH3COOK������������� | |
| D�� | ����90%Fe��NO3��3��Һ����IJ�������������ƿ���ձ�����Ͳ�������� |
���� ����Cl2ͨ���NaOH��Һ�У��¶ȵ�ʱ������ӦCl2+2OH-=Cl-+ClO-+H2O������ҺI�м���NaOH��ʹ������ȫ��Ӧ���ҽ���Һת��Ϊ������Һ��ֻ�м���������ClO-���ܺ�Fe3+����������ԭ��Ӧ����FeO42-����ȥNaCl�õ����Ե�NaClOŨ��Һ������Ե�NaClOŨ��Һ�м���90%��Fe��NO3��3��Һ��������Ӧ2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O���õ���ҺII������Һ�м���KOH���������ͣ��õ�K2FeO4�������õ�ʪ��Ʒ����ʪ��Ʒϴ�ӡ�����õ�����K2FeO4��
A������۷����ķ�ӦΪ2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O��Fe3+�ǻ�ԭ����ClO-����������
B���������Na2FeO4ת��Ϊʪ��Ʒʱ���ܽ�ȴ������ת��Ϊ�ܽ��С�����ʣ�
C�������ˮ�����Һ�ʼ��ԣ������Ƹ����������ˮ�⣬������ܽ���������ܽ����ҷ�ֹ��ˮ�⣻
D������һ��������������Һ����Ҫ����ƿ��
��� �⣺����Cl2ͨ���NaOH��Һ�У��¶ȵ�ʱ������ӦCl2+2OH-=Cl-+ClO-+H2O������ҺI�м���NaOH��ʹ������ȫ��Ӧ���ҽ���Һת��Ϊ������Һ��ֻ�м���������ClO-���ܺ�Fe3+����������ԭ��Ӧ����FeO42-����ȥNaCl�õ����Ե�NaClOŨ��Һ������Ե�NaClOŨ��Һ�м���90%��Fe��NO3��3��Һ��������Ӧ2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O���õ���ҺII������Һ�м���KOH���������ͣ��õ�K2FeO4�������õ�ʪ��Ʒ����ʪ��Ʒϴ�ӡ�����õ�����K2FeO4��
A������۷����ķ�ӦΪ2Fe3++3ClO-+10OH-=2FeO42-+3Cl-+5H2O��Fe3+�ǻ�ԭ����ClO-���������������������ͻ�ԭ�������ʵ���֮��Ϊ3��2����A��ȷ��
B���������Na2FeO4ת��Ϊʪ��Ʒʱ���ܽ�ȴ������ת��Ϊ�ܽ��С�����ʣ��������Na2FeO4ת��Ϊʪ��Ʒ����ΪK2FeO4�ܽ�ȸ�С����B��ȷ��
C�������ˮ�����Һ�ʼ��ԣ������Ƹ����������ˮ�⣬������ܽ���������ܽ����ҷ�ֹ��ˮ�⣬��������е�ϴ�Ӽ�����CH3COOK������������ƣ���C��ȷ��
D������һ��������������Һ����Ҫ����ƿ����Ҫ�ձ�������������Ͳ����D����
��ѡD��
���� ���⿼�������Ʊ����漰������ԭ��Ӧ�����ʷ����ᴿ����Һ���Ƶ�֪ʶ�㣬��ȷʵ��ԭ�����������ʡ����ʷ�����ᴿ�����ǽⱾ��ؼ���ע������һ������������Һ������һ�����ʵ���Ũ����Һ��������������Ŀ�ѶȲ���


 ��ѧʵ����ϵ�д�
��ѧʵ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Zn��s��+CuSO4��aq���TZnSO4��aq��+Cu��s����H=-216 kJ•mol-1��E��Ӧ�E������ | |
| B�� | CaCO3��s���TCaO��s��+CO2��g����H=+178.5 kJ•mol-1��E��Ӧ�E������ | |
| C�� | HI��g���T$\frac{1}{2}$H2��g��+$\frac{1}{2}$I2��s����H=-26.5 kJ•mol-1��1 mol HI���ܱ������зֽ��ų�26.5 kJ������ | |
| D�� | H+��aq��+OH-��aq���TH2O��l����H=-57.2 kJ•mol-1����1 mol NaOHˮ��Һ�뺬0.5 mol��Ũ�����Ϻ����57.2 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ�д�������ƽ��Br2+H2O?HBr+HBrO������AgNO3��Һ����Һ��ɫ��dz | |
| B�� | ��ҵ���������͵����ϳɰ����ڽϸ��¶��½��е� | |
| C�� | SO2��������SO3�ķ�Ӧ����Ҫʹ�ô��� | |
| D�� | H2��I2��HIƽ��������ѹ����ɫ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
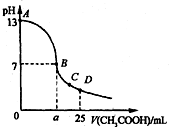 25��ʱ����25mL 0.1mol•L��1��NaOH��Һ�У���μ���0.2mol•L��1��CH3COOH��Һ����ҺpH�ı仯������ͼ��ʾ�����з����Ľ����У�������ǣ�������
25��ʱ����25mL 0.1mol•L��1��NaOH��Һ�У���μ���0.2mol•L��1��CH3COOH��Һ����ҺpH�ı仯������ͼ��ʾ�����з����Ľ����У�������ǣ�������| A�� | C��ʱc��CH3COO������c��Na+����c��H+����c��OH���� | |
| B�� | D��ʱc��CH3COO-��+c��CH3COOH��=2c��Na+�� | |
| C�� | ������A��B����һ�㣬��Һ�ж��У�c��Na+����c��CH3COO������c��OH������c��H+�� | |
| D�� | B������a��12.5 mL |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
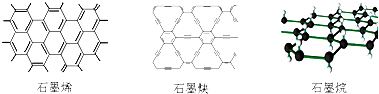
| A�� | ʯīϩ��ʯīȲ��ʯī�黥Ϊͬ�������� | |
| B�� | 12gʯīϩ��ȫת��Ϊʯī��������11.2L | |
| C�� | ʯīȲ�����뵼����ϣ���������������� | |
| D�� | ʯīȲ���Դ���H2���ӵ�ֱ����������������H2�ᴿ��Ĥ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ȶ��ԣ�Na2CO3��NaHCO3 | |
| B�� | �����µ��ܽ��ԣ�Na2CO3��NaHCO3 | |
| C�� | ��ϡ���ᷴӦ�ľ��ҳ̶ȣ�Na2CO3��NaHCO3 | |
| D�� | �������Ĺ�������������ᷴӦ�ų�CO2��������Na2CO3��NaHCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
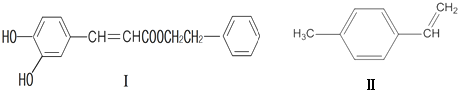
 ��
�� ��д1�֣����ɢ����ɢ�ķ�Ӧ����ΪNaOH�Ĵ���Һ�����ȣ�
��д1�֣����ɢ����ɢ�ķ�Ӧ����ΪNaOH�Ĵ���Һ�����ȣ�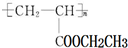 �������Ʊ�Ϳ�ϣ��䵥��ṹ��ʽΪCH2=CHCOOCH2CH3��
�������Ʊ�Ϳ�ϣ��䵥��ṹ��ʽΪCH2=CHCOOCH2CH3���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����40.0LN2������� | B�� | ��0.250molKNO3������ | ||
| C�� | ������0.625mol������ | D�� | ��ת�Ƶ���1.25mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ư����Һ | B�� | ����������Һ | C�� | �Ȼ�����Һ | D�� | �������� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com