
| 实验(混合溶液) | A | B | C | D | E | F |
| 4mol/L 盐酸/mL | 60 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuCl2溶液/mL | 0 | 1.0 | 5.0 | 10 | V6 | 40 |
| H2O/mL | V7 | V8 | V9 | V10 | 20 | 0 |
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 mol/L的NaCl溶液,以胶头滴管加水定容时,液面稍超出容量瓶刻度线,反复摇匀后,凹液面最低点恰好与刻度线相切
mol/L的NaCl溶液,以胶头滴管加水定容时,液面稍超出容量瓶刻度线,反复摇匀后,凹液面最低点恰好与刻度线相切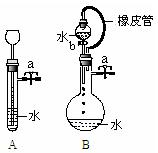
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
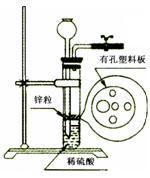
| A.苯 | B. 四氯化碳 | C.酒精 | D.KCl溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.室温下,含有CoCl2的干燥变色硅胶呈蓝色,在潮湿的空气中变粉红色,放在干燥的空气中又恢复为蓝色 |
| B.焰色反应实验中,铂丝在蘸取待测溶液前,应先用稀硫酸洗净并灼烧 |
| C.中和滴定实验中,如用于盛放待测溶液的锥形瓶洗净后未干燥,不影响测定结果 |
| D.纸层析中,滤纸作为固定相,展开剂作为流动相 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
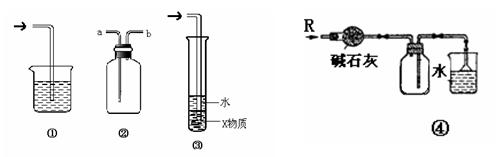
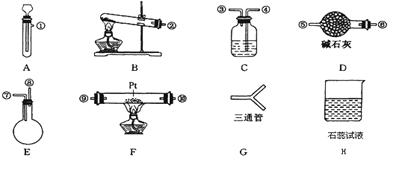
| A.装置①可用于吸收实验中多余的Cl2 |
| B.装置②可用于收集H2、NH3、Cl2、HCl、NO2等 |
| C.装置③中X为苯,可用于吸收氨气或氯化氢 |
| D.装置④可用于收集氨气,并吸收多余的氨气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com