
| A. | 对有气体参加的化学反应,增大压强,体系体积减小,可使单位体积内活化分子数增加 | |
| B. | 升高温度,一般可使活化分子的百分数增大,分子间的碰撞频率提高,因而反应速率增大 | |
| C. | 活化分子之间发生的碰撞一定为有效碰撞 | |
| D. | 加入适宜的催化剂,可使活化分子的百分数大大增加,从而成千上万倍地增大反应速率 |
分析 A、增大压强引起单位体积内活化分子数增大对反应速率的影响进行判断;
B、利用升高温度引起活化分子的百分数增大对反应速率的影响进行判断;
C、活化分子之间发生的碰撞分为有效碰撞和无效碰撞;
D、催化剂降低反应的活化能而使活化分子的百分数大大增加对化学反应速率的影响进行判断.
解答 解:A、增大压强体系体积减小,对于有气体参加的反应,可使单位体积内活化分子数增加,反应速率增大,故A正确;
B、升高温度,反应体系中物质的能量升高,一般可使活化分子的百分数增大,因而反应速率增大,故B正确;
C、由于活化分子之间的碰撞分为有效碰撞和无效碰撞,故C错误;
D、催化剂降低反应的活化能,可使反应需要的能量减小,使活化分子的百分数大大增加,从而成千上万倍地增大化学反应的速率,故D正确;
故选C.
点评 本题考查了外界条件对反应速率的影响,注重了基础知识考查,难度不大.


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:解答题
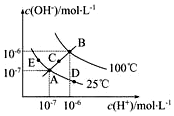 已知水的电离平衡曲线如图示,试回答下列问题:
已知水的电离平衡曲线如图示,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化合反应 | B. | 复分解反应 | C. | 置换反应 | D. | 分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 无色一氧化氮气体与空气接触变为红棕色 | |
| B. | 往盐酸中滴加紫色石蕊试液,溶液变红色 | |
| C. | 向硫酸铜溶液中滴加氢氧化钠溶液,出现白色沉淀 | |
| D. | 将足量二氧化硫气体通入品红溶液,红色逐渐褪去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{vn}{22.4}$ | B. | $\frac{22.4n}{v}$ | C. | $\frac{vn}{5.6}$ | D. | $\frac{22.4n}{3v}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
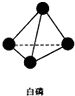 ,并指出1mol白磷(P4)含有P-P键的数目6NA
,并指出1mol白磷(P4)含有P-P键的数目6NA查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 蒸发 | B. | 蒸馏 | C. | 过滤 | D. | 分液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com