
 +3
+3
 2
2 ,则在电化学合成氨的过程中,阴极反应式为_________;
,则在电化学合成氨的过程中,阴极反应式为_________;

 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案科目:高中化学 来源:不详 题型:单选题
 鸡没有汗腺,在夏天只能依赖喘息调节体温。鸡过度呼出CO2,会使下列平衡向左移动,导致蛋壳变薄,使农场主和超市蒙受经济损失。
鸡没有汗腺,在夏天只能依赖喘息调节体温。鸡过度呼出CO2,会使下列平衡向左移动,导致蛋壳变薄,使农场主和超市蒙受经济损失。 CO2(g) CO2(l)
CO2(g) CO2(l) (aq)+
(aq)+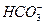 (aq)
(aq) 
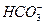 (aq)
(aq) H+(aq)+
H+(aq)+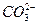 (aq)
(aq)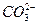 (aq)
(aq) CaCO3(s)
CaCO3(s)| A.淡盐水 | B.碳酸水 | C.蔗糖水 | D.澄清石灰水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

 和NO2反
和NO2反 应可以生成PAN及O2
应可以生成PAN及O2 ),可利用甲烷和NO
),可利用甲烷和NO 在一定条件下反应消除其污染,则CH4与NO2反应的化学
在一定条件下反应消除其污染,则CH4与NO2反应的化学 方程式为 。
方程式为 。 2NO+O3;△H>0,反应过程中浓度随时间变化的情况如下图所示。
2NO+O3;△H>0,反应过程中浓度随时间变化的情况如下图所示。
 4NO2(g)+O2(g)
4NO2(g)+O2(g) 2NO(g)+O2(g)
2NO(g)+O2(g)查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 3C(g) + D(s), 达到平衡时,C的浓度为1.2 mol·L-1。
3C(g) + D(s), 达到平衡时,C的浓度为1.2 mol·L-1。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 压下一个化学反应生成物气体的体积等于反应物气体的体积就可以粗略认为该反应的熵变为0。某化学兴趣小组,专门研究了氧族元素及其某些化合物的部分性质。所查资料如下:
压下一个化学反应生成物气体的体积等于反应物气体的体积就可以粗略认为该反应的熵变为0。某化学兴趣小组,专门研究了氧族元素及其某些化合物的部分性质。所查资料如下: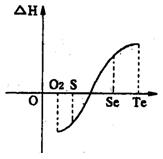
 _____
_____ _____.
_____.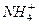 +
+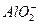 +2H2O
+2H2O Al(OH)3↓ +NH3·H2O,向含有等物质的量的
Al(OH)3↓ +NH3·H2O,向含有等物质的量的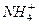 、Al3+、H+混合溶液中,慢慢滴加NaOH溶液,直至过量,并不断搅拌,依次发生了数个离子反应;其中:
、Al3+、H+混合溶液中,慢慢滴加NaOH溶液,直至过量,并不断搅拌,依次发生了数个离子反应;其中: 2HI(g);△H<0。 并达平衡。HI的体积分数HI%随时问变化曲线如图2所示:
2HI(g);△H<0。 并达平衡。HI的体积分数HI%随时问变化曲线如图2所示: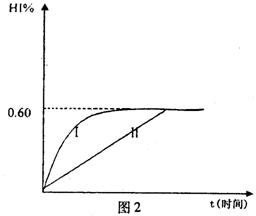
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Ca2+(aq)+2OH-(aq),加入以下物质,可使Ca(OH)2减少的是( )
Ca2+(aq)+2OH-(aq),加入以下物质,可使Ca(OH)2减少的是( )| A.NaCl固体 | B.AlCl3溶液 | C.NaOH溶液 | D.CaCl2固体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C(g)△H<0,随不同温度(T1>T2)。不同压强(P2>P2)或不同时间(t),混合气中C的体积分数C%变化的曲线中,下列图像错误的是( )
2C(g)△H<0,随不同温度(T1>T2)。不同压强(P2>P2)或不同时间(t),混合气中C的体积分数C%变化的曲线中,下列图像错误的是( )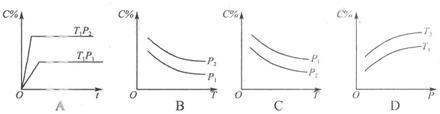
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.1mol/L的某一元酸和0.1mol/L的某一元碱 |
| B.0.1mol/L的某二元强酸和0.1mol/L的某二元碱 |
| C.pH=2的某一元酸和pH=12的某一元碱 |
| D.pH=3的某二元强酸和pH=11的某一元强碱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com