
ij�����ܱ������������淴Ӧ��Z(��)��W(��) X(g)��Y(��) ��H����t1ʱ�̷�Ӧ�ﵽƽ�⣬��t2ʱ����С���������t3ʱ���ٴδﵽƽ��״̬��δ�ٸı������������й�˵������ȷ����
X(g)��Y(��) ��H����t1ʱ�̷�Ӧ�ﵽƽ�⣬��t2ʱ����С���������t3ʱ���ٴδﵽƽ��״̬��δ�ٸı������������й�˵������ȷ����
| A��Z��W�ڸ�������������һ����Ϊ��̬ |
| B��t1��t2ʱ�����t3ʱ�̺���ʱ��η�Ӧ��ϵ�������ƽ��Ħ�������������Ҳ���ܲ��� |
| C�����ڸ��¶��´˷�Ӧƽ�ⳣ������ʽΪK��c(X)����t1��t2ʱ�����t3ʱ�̺��XŨ�Ȳ���� |
| D�����÷�Ӧֻ��ij�¶�T�����Է����У���÷�Ӧ��ƽ�ⳣ��K���¶����߶���С |
B
�������������A������ͼ���֪������Ӧ���ʲ��淴Ӧʱ���ѹǿ�ĸı���ı䣬��Z��W���Dz������壬��A����B�����ͼ���֪�� X�����壬Y���������壬Ҳ���ܲ��ǣ����Է�Ӧ�����������Ħ�������ᷢ���仯����B��ȷ��C�����ڻ�ѧƽ�ⳣ��ֻ���¶��йأ����¶���ƽ�ⳣ���ı���ʽK=c��X���Ƕ�ֵ����t1��t2ʱ�����t3ʱ�̺��c��X����ȣ���C����D�����ڸ÷�Ӧ���¶�ΪT0����ʱ�����Է����У����ݡ�H-T��S��0���ó��÷�Ӧ�����ȷ�Ӧ�������¶�ƽ�������ƶ���ƽ�ⳣ������D����
���㣺���黯ѧƽ���йؼ��㡢��ѧƽ��ͼ��ȣ��ж�t2ʱ�̸ı������ǹؼ��������Ѷ��еȡ�


 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���ܱ������У�ʹ2 mol N2��6 mol H2��Ϸ������з�Ӧ:N2(g)+3H2(g) 2NH3(g)(����ӦΪ���ȷ�Ӧ)������˵���������
2NH3(g)(����ӦΪ���ȷ�Ӧ)������˵���������
| A������ƽ����ϵ���¶�(�����������)����������ƽ����Է���������� |
| B������ƽ����ϵ���¶�(�����������)�����������ܶȲ��䡡 |
| C������Ӧ�ﵽƽ��ʱ��N2��H2��Ũ�ȱ��ǡ�1��3 |
| D�����ﵽƽ��ʱ�����������������ѹǿ���䣬ƽ�⽫�����ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����β�������е�һ����Ӧ���£�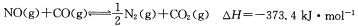
��һ�ݻ�Ϊ5L�ĺ����ܱ������г���0.2 mol NO��0.5mol CO��5 min��÷�Ӧ�ﵽƽ�⣬��ʱN2�����ʵ���Ϊ0.06mol������˵����ȷ����
| A���ﵽƽ�����ֻ�����¶ȣ���ѧƽ�������ƶ� |
| B���ﵽƽ�����ͨ��ϡ�����壬�淴Ӧ�������� |
| C��ʹ�ô�����ƽ�ⳣ������ |
| D��0��5 min�ڣ�NO�ķ�Ӧ����Ϊ2.4��1 0-3 mol��Lһ1��minһ1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
500�������£��ں����ܱ������У�����1molNO2��������ƽ��2NO2(g) N2O4(g) ��ƽ������������ٳ���1molNO2������˵����ȷ��
N2O4(g) ��ƽ������������ٳ���1molNO2������˵����ȷ��
| A��ƽ��������Ӧ�����ƶ� |
| B��ƽ�ⳣ��K���� |
| C��NO2��ת���ʱ�С |
| D��������������ɫ�ȱ�����dz������ԭ����Ҫdz |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�� 4 mol A ����� 2 mol B ������ 2 L �������л�ϲ���һ�������·������·�Ӧ��2A��g����B��g�� 2C��g������ 2 s���룩���� C ��Ũ��Ϊ 0.6 mol��L��1 ���������м���˵����
2C��g������ 2 s���룩���� C ��Ũ��Ϊ 0.6 mol��L��1 ���������м���˵����
�� ������ A ��ʾ�ķ�Ӧ��ƽ������Ϊ 0.3 mol��L��1��S��1
�� ������ B ��ʾ�ķ�Ӧ��ƽ������Ϊ 0.6 mol��L��1��S��1
�� 2 s ʱ���� A ��ת����Ϊ70��
�� 2 s ʱ���� B ��Ũ��Ϊ 0.7 mol��L��1��
������ȷ����
| A���٢� | B���٢� | C���ڢ� | D���ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��1L�ܱ������У���l mol A��1 mol B��Ϸ������·�Ӧ��
3A(g) + B(g)  XC(g) + 2D(g)������Ӧ�ﵽƽ��ʱ������0.4 mol D�������C��ƽ��Ũ��Ϊ0.4 mol/L����������������ȷ����
XC(g) + 2D(g)������Ӧ�ﵽƽ��ʱ������0.4 mol D�������C��ƽ��Ũ��Ϊ0.4 mol/L����������������ȷ����
| A��x��ֵΪ2 | B��A��ת����Ϊ40% |
| C��B��ƽ��Ũ��Ϊ0.8 mol/L | D���ﵽƽ��ʱD���������Ϊ20% |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��һ���¶��µĶ����ܱ������У������ʵ��������������ٱ仯ʱ������˵����Ӧ
A��s����2B��g�� C��g����D��g���Ѵ�ƽ��״̬����
C��g����D��g���Ѵ�ƽ��״̬����
| A����������ѹǿ | B�����������ܶ� |
| C��B�����ʵ���Ũ�� | D�������ƽ����Է������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
һ�������£������Ϊ10 L���ܱ������У�1 mol A��1 mol B���з�Ӧ��2A(g)��B(g) 2C(g)���ﵽƽ��ʱ����0.6 mol C������˵����ȷ����
2C(g)���ﵽƽ��ʱ����0.6 mol C������˵����ȷ����
A�����������ܶȱ��ֲ���ʱ�������жϷ�Ӧ�Ѵ�ƽ��
B�������������䣬�����������Ϊ5 L��C��ƽ��Ũ�ȱ�Ϊԭ����2��
C�������������䣬������ѹǿ��������A��ת���ʼ�С
D���ﵽƽ��ʱ��C������ٷֺ���Ϊ0.353
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ҵ�ϳ��û�ԭ����������������ˮ(Cr2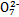 ��Cr
��Cr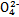 ),������Ϊ:Cr
),������Ϊ:Cr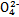
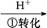 Cr2
Cr2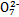
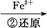 Cr3+
Cr3+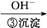 Cr(OH)3��
Cr(OH)3��
��֪:
(1)������д���ƽ��:2Cr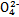 (��ɫ)+2H+
(��ɫ)+2H+ Cr2
Cr2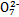 (��ɫ)+H2O
(��ɫ)+H2O
(2)��������ɵ�Cr(OH)3����Һ�д������³����ܽ�ƽ��:
Cr(OH)3(s) Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
(3)������,Cr(OH)3���ܶȻ�Ksp=10-32;�ҵ���Һ������Ũ��С��10-5 mol��L-1ʱ�����������Ӳ�����
�����й�˵������ȷ����(����)
A��������м���,����Һ��pH������2,��Һ�Ի�ɫ,Cr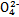 Ũ������ Ũ������ |
B��������е�2v(Cr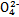 )=v(Cr2 )=v(Cr2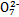 )ʱ,˵����Ӧ2Cr )ʱ,˵����Ӧ2Cr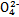 (��ɫ)+2H+ (��ɫ)+2H+ Cr2 Cr2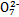 (��ɫ)+H2O�ﵽƽ��״̬ (��ɫ)+H2O�ﵽƽ��״̬ |
C���������,��Ҫ��ԭ1 mol Cr2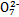 ,��Ҫ12 mol (NH4)2Fe(SO4)2��6H2O ,��Ҫ12 mol (NH4)2Fe(SO4)2��6H2O |
| D���������,������Һ��pH������6ʱ,�����Ϊ��ˮ�еĸ��ѳ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com