
| A. | $\frac{1}{2}$ | B. | $\frac{1}{3}$ | C. | $\frac{1}{4}$ | D. | $\frac{1}{5}$ |
分析 离子的还原性:I->Br->Cl-,由于反应中I-有剩余,则Br-没有被氧化,通入氯气只发生Cl2+2I-=2Cl-+I2,由反应可知,溶液中离子总物质的量不变,故溶液中Br-离子物质的量不变,再利用赋值法,结合离子的物质的量的变化计算.
解答 解:离子的还原性:I->Br->Cl-,由于反应中I-有剩余,则Br-没有被氧化,通入氯气只发生Cl2+2I-=2Cl-+I2,设溶液中Cl-、Br-、I-离子的物质的量分别为2xmol、3xmol、4xmol,由反应后离子物质的量关系可知反应离子的物质的量分别为4xmol、3xmol、2xmol,则Cl-的物质的量增加2xmol,I-的物质的量减少2xmol,则通入氯气xmol,则通入Cl2物质的量与原溶液中I-物质的量之比为x:4x=1:4,即为1:4,
故选:C.
点评 本题考查氧化还原反应的计算,题目难度不大,本题注意把握离子的还原性强弱,判断发生的反应是关键,在根据反应的离子方程式计算.


科目:高中化学 来源: 题型:填空题
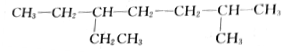 的名称是2-甲基-5-乙基庚烷
的名称是2-甲基-5-乙基庚烷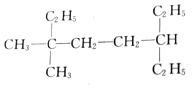 的名称是3,3-二甲基-6-乙基辛烷
的名称是3,3-二甲基-6-乙基辛烷 的名称是2-甲基-3,6-二乙基辛烷
的名称是2-甲基-3,6-二乙基辛烷 的名称是2,4,4,5-四甲基庚烷.
的名称是2,4,4,5-四甲基庚烷.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等浓度CH3COOH溶液与NH3•H2O溶液等体积混合后,存在c(NH4+)+c(H+)=c(CH3COO-)+c(OH-) | |
| B. | 等浓度的HCl溶液与CH3COOH溶液中c(H+)也相同 | |
| C. | 向20mLHCl溶液中加入10mL同一浓度的HCl溶液时,其pH会改变 | |
| D. | 等浓度的CH3COOH溶液和NaOH溶液等体积混合后,溶液显中性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
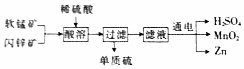 工业上可用软锰矿(主要成分MnO2)和闪锌矿(主要成分为ZnS)制备干电池中所需的MnO2和Zn,其工艺流程如图所示,下列说法中错误的是( )
工业上可用软锰矿(主要成分MnO2)和闪锌矿(主要成分为ZnS)制备干电池中所需的MnO2和Zn,其工艺流程如图所示,下列说法中错误的是( )| A. | 上述流程中锰元素的价态没有变化 | |
| B. | 上述流程中的硫酸可循环利用 | |
| C. | 通电过程中,生成Zn单质时发生还原反应 | |
| D. | 通电过程中,阳极的电极反应式为Mn2+-2e-+2H2O═MnO2+4H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BeCl2溶液pH<7,将其蒸干、灼烧后可得残留物BeCl2 | |
| B. | BeCl2水溶液的导电性强,BeCl2一定是离子晶体 | |
| C. | Be(OH)2能溶于盐酸,不能溶于NaOH溶液 | |
| D. | Na2BeO2溶液pH>7,将其蒸干、灼烧后可得残留物Na2BeO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A、C的氧化物均含离子键 | |
| B. | C离子的半径小于D离子的半径 | |
| C. | A、B可形成多种原子个数比为1:1的化合物 | |
| D. | 含D元素的盐溶液只能显碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作及现象 | 实验目的 | |
| A | 将SO2通入品红溶液中,品红溶液褪色;加热褪色后的品红溶液,溶液恢复红色 | 证明亚硫酸的不稳定性 |
| B | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有少量气泡产生 | 证明常温下KSP(BaCO3)>KSP(BaSO4) |
| C | 常温下测定物质的量浓度相同的盐酸和醋酸溶液的pH:盐酸pH小于醋酸pH | 证明相同条件下,在水中HCl电离程度大于CH3COOH |
| D | 将浓硫酸和碳混合加热,直接将生成的气体通入足量的澄清石灰水,石灰水变浑浊 | 检验气体产物中CO2的存在 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com