
在恒容密闭容器中通入X并发生反应:2X(g) Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是
Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是
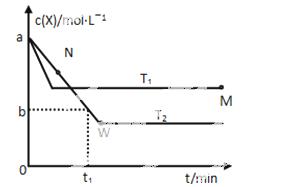
A.该反应进行到M点放出的热量大于进行到W点放出的热量
B.T2下,在0~t1时间内,υ(Y)=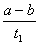 mol/(L·min)
mol/(L·min)
C.M点的正反应速率υ正大于N点的逆反应速率υ逆
D.M点时再加入一定量的X,平衡后X的转化率减小
科目:高中化学 来源: 题型:
蛇纹石矿由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁实验步骤如下:
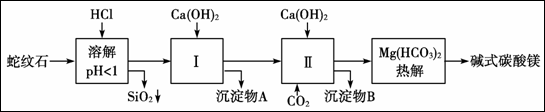
已知:
| 氢氧化物 | Fe(OH) 3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
(1)蛇纹石加盐酸溶解后,溶液里除了Mg2+外,还含有的阳离子有 。
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见上表),Ca(OH)2不能过量,若Ca(OH)2过量可能会导致 溶解、 沉淀。
(3)物质循环使用,能节约资上述实验中,可以循环使用的物质是 。
(4)高温煅烧碱式碳酸镁aMgCO3·bMg(OH)2·cH2O得到MgO。取碱式碳酸镁4.66 g,高温煅烧至恒重,得到固体2.00 g和标准状况下CO2 0.896 L,通过计算确定碱式碳酸镁的化学式为 。(写出计算过程,否则不得分)
查看答案和解析>>
科目:高中化学 来源: 题型:
0.1 mol·L-1 HF溶液的pH=2,则该溶液中有关浓度关系式不正确的是( )
A.c(H+)>c(F-) B.c(H+)>c(HF)
C.c(OH-)<c(HF) D.c(HF)>c(F-)
查看答案和解析>>
科目:高中化学 来源: 题型:
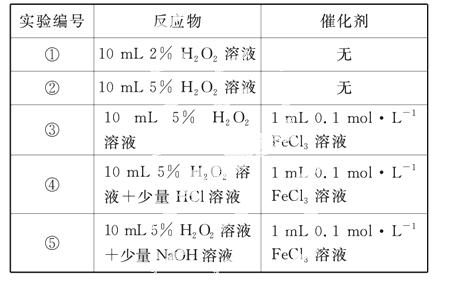
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响。在常温下按照如下方案完成实验。
(1)催化剂能加快化学反应速率的原因是____________。
(2)实验①和②的目的是___________________。
实验时由于没有观察到明显现象而无法得出结论。资料显示,通常条件下H2O2稳定,不易分解。为了达到实验目的,你对原实验方案的改进是__________。
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如下图。
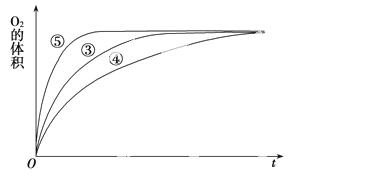
分析上图能够得出的实验结论是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,0.2mol/L一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是
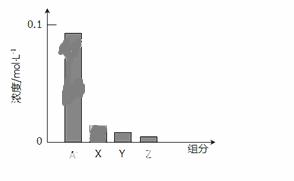
A.HA是强酸
B.该混合液pH=7
C.图中x表示HA,Y表示OH-,Z表示H+
D.该混合溶液中:c(A-)+c(Y)=c(Na+)
查看答案和解析>>
科目:高中化学 来源: 题型:
NaHSO3溶 液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率。将浓度
液在不同温度下均可被过量KIO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率。将浓度 均为0.020 mol·L-1的NaHSO3溶液(含少量淀粉)10.0 mL、KIO3(过量)酸性溶液40.0 mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图。
均为0.020 mol·L-1的NaHSO3溶液(含少量淀粉)10.0 mL、KIO3(过量)酸性溶液40.0 mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图。 据图分析,下列判断不正确的是 ( )
据图分析,下列判断不正确的是 ( )
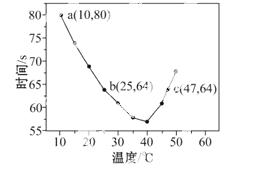
A.40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反
B.图中b、c两点对应的NaHSO3反应速率相等
C.图中a点对应的NaHSO3反应速率为5.0×10-5mol·L-1·s-1
D.温度高于40℃时,淀粉不宜用作该实验的指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)DIS数字化信息系统因为可以准确测量溶液的pH而在中和滴定的研究中应用越来越广泛深入。某学习小组利用DIS系统测定NaOH滴定同浓度HCl、CH3COOH的pH变化曲线分别如下,你能从中得到的信息有(写出2条信息):
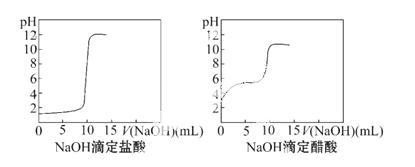
① _______________________________________________;
② _____ __________________________________________。
__________________________________________。
(2) 已知NO2和N2
已知NO2和N2 O4可以相互转化:2NO2(g)
O4可以相互转化:2NO2(g) N
N 2O4(g) ΔH<0。现将一定量NO2和N2O4的混合气体通入一体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图所示,回答下列问题:
2O4(g) ΔH<0。现将一定量NO2和N2O4的混合气体通入一体积为1 L的恒温密闭容器中,反应物浓度随时间变化关系如图所示,回答下列问题:
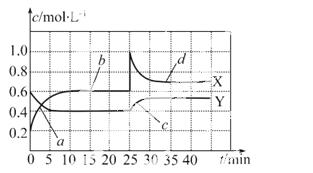
①图中共有两条曲线X和Y,其中曲线 表示NO2浓度随时间的变化;a、b、c、d四个点中,表示化学反应处于平衡状态的点是 __________________。
②前10 min内用NO2表示的化学反 应速率v(NO2)= m
应速率v(NO2)= m ol·L-1·min-1;反应进行至25 min时,曲线发生变化的原因是 ____________________________。
ol·L-1·min-1;反应进行至25 min时,曲线发生变化的原因是 ____________________________。
③若要达到与最后相同的化学平衡状态,在25 min时还可以采取的措施是 __。
A.加入催化剂 B.缩小容器 体积
体积
C.升高温度 D.加入一定量的N2O4
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列说法中正确的是
A.常温常压下,2.3 g Na变成Na2O2时,失去0.2NA个电子
B.常温常压下,32 g氧气和32 g臭氧都含有2NA个氧原子
C.500 mL 0.2 mol/L NaOH溶液中含有NA个Na+离子
D.在20℃、1.01×105Pa时,11.2 L氮气含有NA个氮原子
查看答案和解析>>
科目:高中化学 来源: 题型:
将下列物质按酸、碱、盐分类顺序排列正确的是( )
|
| A. | 硫酸、纯碱、石膏 | B. | 氢硫酸、烧碱、绿矾 |
|
| C. | 醋酸、乙醇、醋酸钠 | D. | 磷酸、熟石灰、苛性钾 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com