
①甲苯 ②乙炔 ③乙烯 ④乙烷 ⑤甲烷⑥苯 ⑦丙烯
A.②③⑦ B.①④⑥ C.②③⑥ D.①④⑤⑦
 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:阅读理解
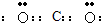
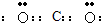


查看答案和解析>>
科目:高中化学 来源: 题型:
 (2010?宝鸡三模)[化学-选修3物质结构与性质]
(2010?宝鸡三模)[化学-选修3物质结构与性质]查看答案和解析>>
科目:高中化学 来源: 题型:
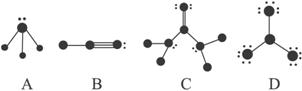
根据各图表示的结构特点,写出该分子的化学式:
A:_______________________; B:_______________________;
C:_______________________; D:_______________________。
(2)在分子的结构式中,由一个原子提供成键电子对而形成的共价键用“→”表示,例如:
硫酸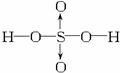 ,硝基甲烷
,硝基甲烷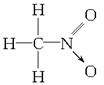 ,
,
写出三硝基甘油酯的结构式:__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)下列物质结构图中,●代表原子序数从1到10的元素的原子实(原子实是原子除去最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表价键,(示例:F2 ![]() )
)
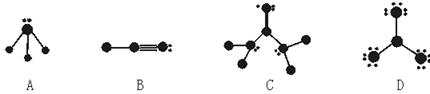
根据各图表示的结构特点,写出该分子的化学式:
A: B: C: D:
(2)在分子的结构式中,由一个原子提供成键电子对而形成的共价键用“→”表示,例如:
 |
硫酸 写出三硝酸甘油酯的结构式:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
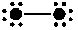 代表原子序数从1到10的元素的原子实(原子实是原子去掉最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表共价键(示例:
代表原子序数从1到10的元素的原子实(原子实是原子去掉最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表共价键(示例: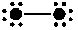 )。
)。
 键的是___________,A中共价键的键角为___________,C的化学键中键长最短的是_________键。
键的是___________,A中共价键的键角为___________,C的化学键中键长最短的是_________键。查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com