
| A | B | C | D | E | F | G | H | I | J | |
| 原子半径(10-10 m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |

分析 前20号元素中,AC都有最低价-2,处于VIA族,A有+6价,C只有-2价,则A为S、C为O元素;E、J都有+4、-4价,处于IVA族,E的原子半径较小,则E是C元素、J是Si;F、I都有+5、-3价,处于VA族,F的原子半径大于I,则F是P元素、I是N元素;G有+7、-1价,为ⅦA族元素,G是Cl元素;D只有+3价,为ⅢA族元素,原子半径大于Si原子半径,所以D是Al元素;B、H最高正价为+1,没有负价,处于IA族,B的原子半径比Al原子半径大很多,不能处于同周期,则B为K,B、H原子半径相差不是太大,应相邻,则H为Na,
(1)同周期自左而右电负性呈增大趋势,同主族自上而下电负性减小;比元素B原子序数大7的元素为Fe,处于第四周期VIII族,结合能量最低原理书写核外电子排布式;
(2)H为Na,I是N,J是Si,其单质的熔点依次升高的为N2<Na<Si;
(3)碳元素、氧元素及氢元素可形成一种相对分子质量为60的一元羧酸分子,该羧酸为CH3COOH;
(4)I与氢元素形成的10电子分子X为NH3,氨气的空间构型为三角锥形,将NH3溶于水后的溶液滴入到CuSO4溶液中至过量,得到络离子的化学式为[Cu (NH3)4]2+,其中NH3与Cu2+之间以配位键结合;
(5)图1是I元素形成的含氧酸的结构,则该酸为HNO3,根据相似形溶原理和氢键分析;
(6)J是Si,E是C,以晶胞顶点上的Si为例,与之距离最近的Si为12,晶胞内Si原子数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,晶胞内C原子数目为4,晶胞边长为a cm,则晶胞的体积为a3,据此计算铜原子半径.
解答 解:(1)同周期自左而右电负性呈增大趋势,同主族自上而下电负性减小,故上述元素中电负性最大的元素是氧元素;比元素B原子序数大7的元素为Fe,处于第四周期VIII族;基态原子核外电子排布为:1s22s22p63s23p63d64s2(或[Ar]3d64s2);
故答案我为:O;4;VIII;1s22s22p63s23p63d64s2(或[Ar]3d64s2);
(2)H为Na,I是N,J是Si,其单质的熔点依次升高的为N2<Na<Si;
故答案为:N2<Na<Si;
(3)碳元素、氧元素及氢元素可形成一种相对分子质量为60的一元羧酸分子,该羧酸为CH3COOH,其分子中共形成7个σ键,1个π键;
故答案为:7;1;
(4)X为NH3,NH3中氮原子的价层电子对数为$\frac{5+3}{2}$=4,有一对孤电子对,所以NH3空间构型为三角锥形,将NH3溶于水后的溶液滴入到CuSO4溶液中至过量,得到络离子的化学式为[Cu (NH3)4]2+,其中NH3与Cu2+之间以配位键结合;
故答案为:三角锥形;[Cu (NH3)4]2+;配位;
(5)图1中的含氧酸为HNO3,HNO3易溶于水的原因a.HNO3是极性分子,易溶于极性的水中;b.HNO3分子中的-OH易与水分子之间形成氢键;
故答案为:HNO3是极性分子,易溶于极性的水中; HNO3分子中的-OH易与水分子之间形成氢键;
(6)J是Si,E是C,以晶胞顶点上的Si为例,与之距离最近的Si为12,晶胞内Si原子数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,晶胞内C原子数目为4,晶胞边长为a cm,则晶胞的体积为a3,晶体的密度为$\frac{4×M(SiC)}{{a}^{3}{N}_{A}}$g/mL=$\frac{4×40}{{a}^{3}{N}_{A}}$g/mL=$\frac{160}{{a}^{3}{N}_{A}}$g/mL;
故答案为:12;$\frac{4×M(SiC)}{{a}^{3}{N}_{A}}$或$\frac{4×40}{{a}^{3}{N}_{A}}$或$\frac{160}{{a}^{3}{N}_{A}}$.
点评 本题考查元素周期表与元素周期律的综合应用,为高考常见题型,侧重对学生分析能力的考查,注意把握原子半径的递变规律、化合价与位置关系,确定元素是解答关键,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 27.5 g•mol-1 | B. | 55 g•mol-1 | C. | 100 g•mol-1 | D. | 111 g•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.6 mol•L-1 | B. | 0.8 mol•L-1 | C. | 0.3 mol•L-1 | D. | 0.4 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 CH3COOC2H5+H2O;该反应的有机反应类型是取代(酯化)反应.
CH3COOC2H5+H2O;该反应的有机反应类型是取代(酯化)反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
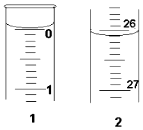 某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:
某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂.请填写下列空白:| 滴定 次数 | 待测氢氧化钠溶 液的体积/mL | 0.1000mol•L+1盐酸的体积(mL) | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 25.00 | 0.00 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 |
| 第三次 | 25.00 | 0.22 | 26.31 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径由大到小的顺序为R、Z、Y、W | |
| B. | X、Y分别与Z形成的多种化合物中化学键类型相同 | |
| C. | Y、R分别与X形成的化合物沸点依次升高 | |
| D. | Z、W、R最高价氧化物对应的水化物两两之间均能发生反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com