
【题目】工业综合处理含![]() 废水和含
废水和含![]() 的废气,得无毒气体b,流程如下:
的废气,得无毒气体b,流程如下:
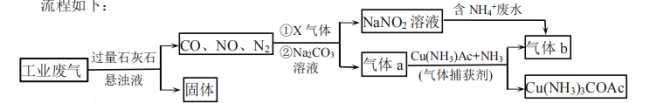
下列说法错误的是( )
A.“固体”中主要含有![]() 、
、![]()
B.X气体、![]() 与
与![]() 溶液的离子反应:
溶液的离子反应:![]()
C.处理含![]() 废水时,离子反应:
废水时,离子反应:![]()
D.捕获剂捕获气体a中![]() 发生了氧化还原反应
发生了氧化还原反应
【答案】D
【解析】
A.工业废气通入过量的石灰石悬浊液,二氧化硫被吸收形成亚硫酸钙沉淀,所以固体中含有碳酸钙和亚硫酸钙,故A正确;
B.由题中信息可知,一氧化氮能被碳酸钠吸收成亚硝酸钠,氮元素的化合价由+2升高到+3,故需要加入氧化剂,结合所涉及的元素可知,通入的X为氧气,离子反应:![]() ,B正确;
,B正确;
C.亚硝酸钠中的氮元素为+3价,与铵根离子中的-3价氮元素发生氧化还原反应,生成的无污染的气体为氮气,根据电子转移守恒和电荷守恒分析,其方程式为NH4++NO2-==N2↑+2H2O,C正确;
D.一氧化碳、N2与碳酸钠不反应,根据反应前后的物质变化可知,捕获剂捕获的气体主要为CO,产物为Cu(NH3)3COAC,反应前后碳和氧的化合价没有变,故该反应不是氧化还原反应,D错误。
答案选D。


科目:高中化学 来源: 题型:
【题目】下列反应属于氧化还原反应,且在反应中水只作为还原剂的是( )
A.3Fe+4H2O(g)![]() Fe3O4+4H2B.2H2O
Fe3O4+4H2B.2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
C.Na2O+H2O═2NaOHD.2F2+2H2O═4HF+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验室做铜与浓硫酸反应的实验。
(1)写出反应的化学方程式_____。
停止加热,将试管中的混合物冷却后倒入装有冷水的烧杯中,搅拌、静置,观察到烧杯底部有黑色物质。于是他对黑色物质进行了探究。
(2)该同学假设黑色物质CuO。检验过程如下:
(查阅文献:检验微量Cu2+的方法是:向试液中滴加K4[Fe(CN)6]溶液,若产生红褐色沉淀,证明有Cu2+)该同学的实验操作:
①将CuO放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,产生红褐色沉淀。
②将黑色物质放入稀硫酸中,一段时间后,滴加K4[Fe(CN)6]溶液,未见红褐色沉淀。实验①的目的是__________,由该检验过程所得结论是________。
(3)再次假设,黑色物质是铜的硫化物。实验如下:
实验装置
| 现象 1.A试管中黑色沉淀逐渐溶解 2.A试管内上方出现浅红棕色气体 3.B试管中出现…… |
①现象2说明黑色物质具有________性。
② A试管内上方出现浅红棕色气体的化学方程式是__________。
③能确认黑色沉淀中含有S元素的现象_________。
(4)以上实验说明,黑色物质中存在铜的硫化物。进一步实验后证明黑色物质是 CuS与Cu2S的混合物。已知1molCu2S与稀硝酸反应转移8mole-,写出试管A中Cu2S 溶解的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】药物吗替麦考酚酯有强大的抑制淋巴细胞增殖的作用,可通过如下反应制得:
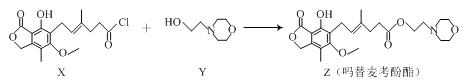 +HCl
+HCl
下列叙述正确的是
A. 用溴水可鉴别化合物X和ZB. 化合物Y的分子式为C6H14NO2
C. 化合物Z中含有手性碳原子D. 1mol化合物Z可以与3mol NaOH反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质中只有A、B、C三种单质,A的焰色反应为黄色,主要以G形式存在于海水中,F是一种淡黄色的固体,H是一种常见的无色液体,I是造成温室效应的“元凶”,各物质间的转化关系图如下:
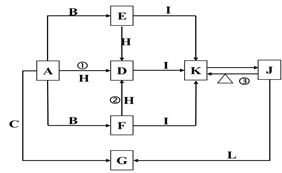
回答下列问题:
(1)A是:____________, I是:____________(填化学式);
(2)按要求写出下列反应的方程式:
Ⅰ.①的化学方程式:______________________________;
Ⅱ.②的化学方程式(同时用双线桥法表示该反应的电子转移情况):________________;
Ⅲ. J与过量的澄清石灰水反应的离子方程式:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 4gNaOH固体所含电子总数为2NA
B. 22.4LC2H6所含化学键总数为7NA
C. 6gSiO2所含分子数为0.1NA,化学键总数为0.4NA
D. 0.1mol·L-1NH4Cl溶液中,![]() 与Cl-数之和小于0.2NA
与Cl-数之和小于0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某无机化合物的二聚分子(小球大小只代表种类不同,与原子半径大小无关),该分子中A、B两种元素都是第3周期的元素,分子中所有原子的最外层电子数都达到8个电子的稳定结构。下列说法不正确的是 ( )

A. 该化合物的化学式是Al2Cl6
B. 该化合物是离子化合物,在熔融状态下能导电
C. 该化合物在固态时所形成的晶体是分子晶体
D. 该化合物中不存在离子键,也不含有非极性共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在100mL 0.10 mol·L-1的 AgNO3溶液中加入100mL溶有2.08g BaCl2的溶液,再加入100 mL溶有0.010 mol CuSO4·5H2O的溶液,充分反应。下列说法中正确的是( )
A. 最终得到白色沉淀和无色溶液
B. 最终得到的白色沉淀是等物质的量的两种化合物的混合物
C. 在最终得到的溶液中,Cl—的物质的最为0.02 mol
D. 在最终得到的溶液中,Cu2+的物质的量浓度为0.01 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量的铝铁合金与1000mL一定浓度的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4.00mol/L的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。试回答下列问题:
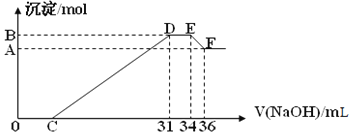
(1)原混合物中铝粉与铁粉的物质的量之比为______
(2)硝酸溶液的物质的量浓度为______molL-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com