
【题目】化学反应基本原理不仅具有理论意义,而且具有实用价值。
(1)为了减轻大气污染,人们提出通过以下反应来处理汽车尾气:
2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H
N2(g)+2CO2(g) △H
已知:①N2(g)+O2(g)=2NO(g) △H1=+ 180.5kJ/mol
②2C(s)+O2(g)=2CO(g) △H2=-221.0kJ/mol
③C(s) +O2(g)=CO2(g) △H3=-393.5kJ/mol
则△H=______kJ/mol
(2)工业上常用反应CO(g) +2H2(g)![]() CH3OH(g) △H=-90.7kJ/mol 合成甲醇,恒温恒容条件下,能说明该反应一定达到平衡状态的是_____(填字母)。
CH3OH(g) △H=-90.7kJ/mol 合成甲醇,恒温恒容条件下,能说明该反应一定达到平衡状态的是_____(填字母)。
a.混合气体的密度不再随时间改变
b.气体的总压强不再随时间改变
c.CO和CH3OH 的浓度之比不再随时间改变
d.v消耗(CO)=v生成(CH3OH)
(3)草木灰是农家肥料,它的主要成分是碳酸钾,其水溶液显____(填“ 酸性”、“ 碱性”或“ 中性”),原因是___________(用离子方程式表示)。
(4)向含有相同浓度Fe2+、Hg+的溶液中滴加Na2S溶液,先生成______沉淀(填化学式)。在工业废水处理过程中,依据沉淀转化原理,可用FeS作为沉淀剂除去废水中的Hg2+,写出相应的离子方程式___________________。(Ksp(FeS)=6.3×10-18,Ksp(HgS)=6.4×10-53)
【答案】 -746.5 bc 碱性 CO32-+H2O![]() HCO3-+OH- HCO3-+H2O
HCO3-+OH- HCO3-+H2O![]() H2CO3+OH-(可以只写第一步) HgS FeS(s)+Hg2+(aq)=HgS(s)+Fe2+(aq)
H2CO3+OH-(可以只写第一步) HgS FeS(s)+Hg2+(aq)=HgS(s)+Fe2+(aq)
【解析】 (1) ①N2(g)+O2(g)=2NO(g) △H1=+180.5kJ/mol;②2C(s)+O2(g)=2CO(g) △H2=-221.0kJ/mol;③C(s)+O2(g)=CO2(g) △H3=-393.5kJ/mol。由③![]() -①-②得,2NO(g)+2CO(g)
-①-②得,2NO(g)+2CO(g)![]() N2(g)+2CO2(g),所以△H=2△H3-△H1-△H2=2
N2(g)+2CO2(g),所以△H=2△H3-△H1-△H2=2![]() (-393.5kJ/mol) -180.5kJ/mol -(-221.0kJ/mol)= -746.5kJ/mol。
(-393.5kJ/mol) -180.5kJ/mol -(-221.0kJ/mol)= -746.5kJ/mol。
(2)工业上常用反应CO(g)+2H2(g)![]() CH3OH(g) △H=-90.7kJ/mol合成甲醇,该反应为反应前后气体分子数不等的放热反应。恒温恒容条件下,a.因为气体的总质量和总体积保持不变,故混合气体的密度一直不变,不能由密度判断该反应的平衡状态; b.气体的总压强不再随时间改变,能说明达到平衡状态;c.CO和CH3OH的浓度之比不再随时间改变,能说明反应达到平衡;d.v消耗(CO)=v生成(CH3OH)只表示了正反应速率,不能说明正反应速率和逆反应速率相等,无法由此判断平衡状态。综上所述,能说明该反应一定达到平衡状态的是bc。
CH3OH(g) △H=-90.7kJ/mol合成甲醇,该反应为反应前后气体分子数不等的放热反应。恒温恒容条件下,a.因为气体的总质量和总体积保持不变,故混合气体的密度一直不变,不能由密度判断该反应的平衡状态; b.气体的总压强不再随时间改变,能说明达到平衡状态;c.CO和CH3OH的浓度之比不再随时间改变,能说明反应达到平衡;d.v消耗(CO)=v生成(CH3OH)只表示了正反应速率,不能说明正反应速率和逆反应速率相等,无法由此判断平衡状态。综上所述,能说明该反应一定达到平衡状态的是bc。
(3)草木灰是农家肥料,它的主要成分是碳酸钾,其水溶液显碱性,原因是碳酸根离子发生水解而使溶液显碱性,该反应的离子方程式为CO32-+H2O![]() HCO3-+OH- 、HCO3-+H2O
HCO3-+OH- 、HCO3-+H2O![]() H2CO3+OH-。
H2CO3+OH-。
(4)向含有相同浓度Fe2+、Hg+的溶液中滴加Na2S溶液,因为Ksp(FeS) >Ksp(HgS),所以先生成HgS沉淀。在工业废水处理过程中,依据沉淀转化原理,可用FeS作为沉淀剂除去废水中的Hg2+,相应的离子方程式为FeS(s)+Hg2+(aq)=HgS(s)+Fe2+(aq)。


 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
【题目】将金属铜投入金属甲的盐溶液中,观察到铜的表面出现银白色物质;金属乙投入稀硫酸中,观察到乙的表面有气泡产生。下列关于金属甲、乙、铜活动性顺序的叙述正确的是( )
A.乙>铜>甲B.甲>铜>乙
C.乙>甲>铜D.甲>乙>铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.在氧化还原反应中,氧化剂经化学变化变成还原剂
B.在氧化还原反应中,氧化剂被氧化,还原剂被还原
C.在化学反应中,能把其他物质氧化的物质是氧化剂
D.在氧化还原反应中,还原剂生成的氧化产物一定只具有氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有3份等质量的小苏打,第1份直接与盐酸恰好完全反应;第2份首先加热,使其部分分解后,再与盐酸恰好完全反应;第3份首先加热,使其完全分解后,再与盐酸恰好完全反应。假若盐酸的物质的量浓度相同,消耗盐酸的体积分别为V1、V2和V3,则V1、V2和V3的大小关系正确的是( )
A.V1>V2>VB.V1>VC.V2>V3>V1D.V1=V2=V3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O反应中,下列说法正确的是
A. 氧化产物与还原产物物质的量之比5∶2
B. 2mol KMnO4完全反应,转移的电子数为16NA
C. 该反应中HCl做还原剂,KCl、MnCl2是氧化产物
D. 氧化剂与还原剂的物质的量之比5∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图所示装置进行实验,填写有关现象及化学方程式。
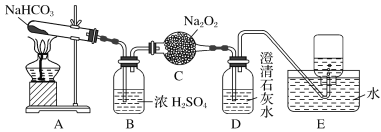
(1) D中的现象是______________,E中收集的气体是_________ (填名称)。
(2) A中发生反应的化学方程式为____________________________________________。
(3) C中发生反应的化学方程式为__________________________________________、
______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量Na2CO3和NaHCO3的均匀混合物分成等量的两份。将其中的一份直接加热至恒重,质量减轻了1.24 g;另一份加入一定量某浓度的盐酸至恰好反应完全,收集到标准状况下2.24 L 气体。则混合物中Na2CO3和NaHCO3的物质的量之比为
A. 1︰3 B. 3︰2 C. 1︰1 D. 2︰3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2017年中国首次海域可燃冰(CH4·nH2O,密度ρ1g·cm-3)试开采成功。若以辛烷代表汽油(密度ρ2g·cm-3)的组成,下列说法不正确的是
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H 1=-a kJ·mol-1
②2C8H18(l)+25O2(g)=16CO2(g)+18H2O(l)△H2 =-bkJ·mol-1
A. 可燃冰适宜保存在低温,高压的环境中
B. 1m3可燃冰可释放出标准状況下[22.4ρ1/(16+18n)]m3的CH4
C. 汽油的燃烧热约为0.5b kJ·mol-1
D. 1m3可燃冰释放出的甲烷燃烧放出的热量约为等体积汽油的[228aρ1/(16+18n)bρ2]倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com