
| 操 作 | 现 象 | 结 论 | |
| A | 取久置的Na2O2粉末,向其中滴加过量的盐酸 | 产生无色气体 | Na2O2没有变质 |
| B | 将一片铝箔置于酒精灯外焰上灼烧 | 铝箔熔化 但不滴落 | 铝箔表面有致密Al2O3薄膜,且Al2O3熔点高于Al |
| C | 无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| D | 向溶液X中加入稀盐酸,并将产生的无色无味气体通入澄清石灰水中 | 生成白色沉淀 | 溶液X中可能含有 CO32-或 HCO3- |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Na2O2粉末及变质生成的碳酸钠均能与盐酸反应生成气体;
B.氧化铝的熔点高,包裹在Al的外面;
C.氯水中的氯气和碘离子反应生成碘单质,四氯化碳把碘从水溶液中萃取出来而显紫色;
D.无色无味气体为二氧化碳.
解答 解:A.Na2O2粉末及变质生成的碳酸钠均能与盐酸反应生成气体,所以不能说明是否完全变质,故A错误;
B.将一片铝箔置于酒精灯外焰上灼烧生成氧化铝,氧化铝的熔点高,包裹在Al的外面,则铝箔熔化但不滴落,故B正确;
C.原溶液为无色溶液说明原溶液中无碘单质,氯水中的氯气和碘离子反应生成碘单质,四氯化碳把碘从水溶液中萃取出来,四氯化碳密度比水大,下层溶液显紫色,所以滴加氯水和四氯化碳,下层溶液显紫色说明原溶液中有碘离子,故C正确;
D.无色无味气体为二氧化碳,可说明含SO32-或HSO3-,故D正确.
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及氧化性强弱判断、离子检验等知识点,综合考查学生的分析能力、实验能力和评价能力,知道碘离子、碳酸根等的检验方法和现象,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 用纯碱溶液清洗油污时,加热可以增强其去污能力 | |
| B. | 在配制FeCl2溶液,可加入少量的盐酸,目的是防止Fe2+被氧化 | |
| C. | TiCl4+(x+2)H2O?TiO2•XH2O+4HCl.在用 TiCl4制备TiO2反应中,加入大量的水,同时加热,可以促进反应趋于完全 | |
| D. | 工业原料氯化铵中含杂质氯化铁,使其溶解于水,在加入氨水调节pH至7~8,可以使Fe3+生成Fe(OH)3沉淀而除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度能够增加活化分子的总数 | |
| B. | 增大反应物浓度能够增加活化分子的百分数 | |
| C. | 加入催化剂可以使本来不能发生的反应发生化学反应 | |
| D. | 压强影响所有化学反应的速率 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某溶液中滴入AgNO3溶液,生成白色沉淀,该溶液中可能含Cl- | |
| B. | 实验已经证明,氯水是可以导电的,所以氯水是电解质 | |
| C. | 某溶液与淀粉碘化钾溶液反应后出现蓝色,则证明该溶液是氯水 | |
| D. | 胶体与其它分散系的本质区别在于胶体具有丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液氨汽化时要吸收大量的热,可用作制冷剂 | |
| B. | SiO2既能与HF反应,又能与NaOH反应,属于两性氧化物 | |
| C. | CO、NO、NO2都是大气污染气体,在空气中都能稳定存在 | |
| D. | 氯化铝是一种电解质,可用于电解制铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用焰色反应鉴别NaCl、KCl | |
| B. | 用氢氧化钠溶液鉴别MgCl2溶液、AlCl3溶液 | |
| C. | 利用稀硫酸鉴别SiO2与Al2O3固体 | |
| D. | 用氢氧化钙溶液鉴别Na2CO3和NaHCO3两种溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 实验序号 | 实验操作 | 现象 | 结论 |
| Ⅰ | 向氯水中加入淀粉KI溶液 | 溶液变蓝 | 氯水中含有氯气分子 |
| Ⅱ | 将氯水滴入AgNO3溶液 | 产生白色沉淀 | 氯气与水反应的产物中含有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
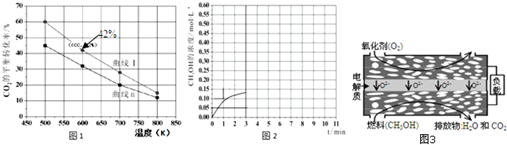
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com