
【题目】(1)工业上利用N2和H2合成NH3,NH3又可以进一步制备联氨(N2H4)等。由NH3制备N2H4的常用方法是NaClO氧化法,其离子反应方程式为___________,有学者探究用电解法制备的效率,装置如图,试写出其阴极电极反应式__________________;

(2)某种铅酸蓄电池具有廉价、长寿命、大容量的特点,它使用的电解质是可溶性的甲基磺酸铅,电池的工作原理:Pb+PbO2+4H+![]() 2Pb2++2H2O充电时,阳极的电极反应式为_________;
2Pb2++2H2O充电时,阳极的电极反应式为_________;
(3)乙醇汽油是被广泛使用的新型清洁燃料,工业生产乙醇(CH3CH2OH)的一种反应原理为:2CO(g)+4H2(g)![]() CH3CH2OH(g)+H2O(g) △H=-akJ/mol
CH3CH2OH(g)+H2O(g) △H=-akJ/mol
己知:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-bkJ/mol
CO2(g)+H2(g) △H=-bkJ/mol
以CO2(g)与H2(g)为原料也可合成乙醇,并放出热量,写出该反应的热化学反应方程式:___________。
(4)如图是一个电化学过程的示意图。

请回答下列问题:
![]() 写出通入CH3OH的电极的电极反应式______。
写出通入CH3OH的电极的电极反应式______。
②乙池中C棒电极反应的方程式为__________________,当乙池中B极质量增加10.8g,此时丙池中析出3.2g某金属,则丙池中的某盐溶液可能是______(填序号)
A.MgSO4溶液 B.CuSO4溶液 C.NaCl溶液 D.AgNO3溶液
【答案】2NH3+ClO- =N2H4+H2O + Cl- O2+4e-=2O2- Pb2++2H2O-2e- =PbO2+4H+ 2CO2(g)+6H2(g)=C2H5OH(g)+3H2O(g) △H=-(a-2b) kJ/mol CH3OH-6e-+8OH-=CO32-+6H2O 2H2O-4e-=O2↑+4H+ BD
【解析】
根据装置特点判断是原电池还是电解池,根据原电池和电解池原理分析正负极和阴阳极并书写对应的电极反应式;根据盖斯定律书写热化学方程式;根据二次电池的总反应,书写电极反应;根据闭合回路中电子转移守恒计算电极产物的量。
(1)根据题干信息知NH3被NaClO氧化生成N2H4,NaClO被还原生成Cl-,离子方程式为:2NH3+ClO- =N2H4+H2O + Cl-;根据电解装置分析知,阴极发生还原反应,元素化合价降低,装置中左侧为阴极,氧气得电子生成氧离子,电极反应为:O2+4e-=2O2-,故答案为:2NH3+ClO- =N2H4+H2O + Cl-;O2+4e-=2O2-;
(2)根据Pb+PbO2+4H+![]() 2Pb2++2H2O分析得,充电时,阳极失电子,发生氧化反应,元素化合价升高,则电极反应式为:Pb2++2H2O-2e- =PbO2+4H+;
2Pb2++2H2O分析得,充电时,阳极失电子,发生氧化反应,元素化合价升高,则电极反应式为:Pb2++2H2O-2e- =PbO2+4H+;
(3)根据盖斯定律得:2CO(g)+4H2(g)![]() CH3CH2OH(g)+H2O(g) △H1=-akJ/mol I,CO(g)+H2O(g)
CH3CH2OH(g)+H2O(g) △H1=-akJ/mol I,CO(g)+H2O(g)![]() CO2(g)+H2(g) △H2=-bkJ/mol II,I-2×II得:2CO2(g)+6H2(g)=C2H5OH(g)+3H2O(g) △H=△H1-2△H2=-(a-2b) kJ/mol;
CO2(g)+H2(g) △H2=-bkJ/mol II,I-2×II得:2CO2(g)+6H2(g)=C2H5OH(g)+3H2O(g) △H=△H1-2△H2=-(a-2b) kJ/mol;
(4)![]() 根据图示,甲池为甲醇燃料电池,通入甲醇的电极为负极,发生氧化反应,因为电解质为KOH,所以氧化产物为碳酸钾,电极反应式为:CH3OH-6e-+8OH-=CO32-+6H2O;
根据图示,甲池为甲醇燃料电池,通入甲醇的电极为负极,发生氧化反应,因为电解质为KOH,所以氧化产物为碳酸钾,电极反应式为:CH3OH-6e-+8OH-=CO32-+6H2O;
②乙池为电解池,C棒连接电池的正极,阳极失电子发生氧化反应,根据放电顺序,水失电子生成氧气和氢离子,电极反应的方程式为: 2H2O-4e-=O2↑+4H+;乙池中B极反应为Ag++e-=Ag,质量增加10.8g,则转移电子数为![]() =0.1mol;丙池某电极析出3.2g金属,说明丙池中电解质是含有氧化性较强的金属阳离子在阴极得电子析出金属,不可能是镁离子和钠离子的盐溶液,则AC错误;此时转移电子为0.1mol,若是二价金属,金属的摩尔质量是
=0.1mol;丙池某电极析出3.2g金属,说明丙池中电解质是含有氧化性较强的金属阳离子在阴极得电子析出金属,不可能是镁离子和钠离子的盐溶液,则AC错误;此时转移电子为0.1mol,若是二价金属,金属的摩尔质量是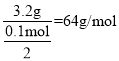 ,所以电解质是含有铜离子的盐溶液,则B正确;若是一价金属,金属的摩尔质量是32g/mol,但题目中没说丙池盐溶液足量,若AgNO3不足,只能电解出3.2gAg,之后一直电解水,所以D正确,故答案为:2H2O-4e-=O2↑+4H+;BD。
,所以电解质是含有铜离子的盐溶液,则B正确;若是一价金属,金属的摩尔质量是32g/mol,但题目中没说丙池盐溶液足量,若AgNO3不足,只能电解出3.2gAg,之后一直电解水,所以D正确,故答案为:2H2O-4e-=O2↑+4H+;BD。


科目:高中化学 来源: 题型:
【题目】如图分别表示生物体内的生物大分子的部分结构模式图,据图回答下列问题:

(1)图甲中的三种物质的基本单位都是__________,其中属于动物细胞储能物质的是____________。
(2)图乙化合物是肺炎双球菌遗传物质的一部分结构示意图,其基本单位是______________,可用图中字母______________表示。
(3)图丙所示化合物的名称是____________,连接氨基酸的化学键是____________(填化学键结构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知Cr2+不稳定,极易被氧气氧化,不与锌反应。醋酸亚铬水合物[Cr(CH3COO)2]2·2H2O是一种深红色晶体,不溶于冷水,是常用的氧气吸收剂。实验室中以锌粒、CrCl3溶液、CH3COONa溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如下图所示。制备过程中发生的相关反应如下所示:
Zn+2HCl===ZnCl2+H2↑
Zn+2CrCl3===2CrCl2+ZnCl2
2Cr2++4CH3COO-+2H2O===[Cr(CH3COO)2]2·2H2O(晶体)

试回答下列问题:
(1)本实验中配制溶液所用的蒸馏水需事先煮沸,原因是__________。
(2)往仪器Ⅱ中加盐酸和CrCl3溶液的顺序最好是__________________________,理由是____________。
(3)为使生成的CrCl2溶液与CH3COONa溶液混合,应关闭阀门____(填“A”或“B”,下同),打开阀门_____。
(4)本实验中锌粒要过量,其原因除了使锌与CrCl3充分反应得到CrCl2外,另一个作用是________。仪器Ⅳ的主要作用是___________。
(5)已知实验时取用的CrCl3溶液中含溶质9.51 g,取用的CH3COONa溶液为1.5 L 0.1 mol/L,其他反应物足量。实验后得干燥的[Cr(CH3COO)2]2·2H2O 9.4 g,则该实验所得产品的产率为________(用百分数表示,保留3位有效数字)(不考虑溶解的醋酸亚铬水合物)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在3个容积均为![]() 的恒容密闭容器中反应
的恒容密闭容器中反应![]() 达到平衡,下列说法正确的是
达到平衡,下列说法正确的是
容器 | 温度 | 物质的起始浓度 | 物质的平衡浓度 | ||
|
|
|
| ||
Ⅰ | 400 |
|
| 0 |
|
Ⅱ | 400 |
|
| 0 |
|
Ⅲ | 500 |
|
| 0 |
|
A. 该反应的正反应是吸热反应
B. 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的小
C. 达到平衡时,容器Ⅱ中![]() 小于容器Ⅲ中
小于容器Ⅲ中![]()
D. 达到平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述中,不正确的是
A.  精炼铜,则a极为粗铜,电解质
精炼铜,则a极为粗铜,电解质![]() 溶液浓度不变
溶液浓度不变
B.  总反应是:
总反应是:![]()
C.  中辅助阳极应为惰性电极
中辅助阳极应为惰性电极
D.  铁钉几乎没被腐蚀
铁钉几乎没被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,A是由X和Y两种短周期元素组成的气体,X的原子序数小于Y,甲、乙、丙分别是X、Y、Z元素对应的单质,Z是地壳中含量最高的元素,它们有如右图所示的转化关系。下列说法不正确的是

A. X、Y、Z三种元素能组成离子化合物
B. 反应②为化合反应,反应③为置换反应
C. 常温常压下,Z的简单氢化物的熔沸点为同族最高
D. 原子半径:Y>Z>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三盐基硫酸铅(3PbO·PbSO4·H2O)简称“三盐”,白色或微黄色粉末,热稳定性能优良,主要用作聚氯乙烯的热稳定剂。“三盐”是由可溶性铅盐中加入硫酸生成硫酸铅,再加氢氧化钠而制得。以100.0吨铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如下图所示

已知:(1)Ksp(PbSO4)=1.82×10-8,Ksp(PbCO3)=1.46×10-13;
(2)铅与冷盐酸、冷硫酸几乎不起作用。
请回答下列问题:
(1)写出步骤①“转化”的化学方程式_________________________________
(2)步骤②“过滤1”后所得滤渣的主要成分为_____________
(3)步骤③“酸溶”,最适合选用的酸为___________,为提高酸溶速率,可采取的措施是____________________________________(任意写出一条)
(4)若步骤④“沉铅”后的滤液中c(Pb2+)=1.82×10-5mol·L-1,则此时c(SO42-)=_________ mol·L-1
(5)从原子利用率的角度分析该流程的优点为____________________________________。
(6)步骤⑥“合成”三盐的化学方程式为____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能证明铝的金属性比镁弱的实验事实是( )
A.镁与冷的浓硫酸反应,铝与冷的浓硫酸不反应
B.铝的原子半径比镁小
C.Al(OH)3能溶于NaOH溶液,而Mg(OH)2不能
D.银的金属光泽不如镁显著
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com